一、<b >选择题(每小题</b><b >2</b><b>分,共</b><b>20</b><b >分,每题只有一个符合题意)</b>
-
1.
下列变化过程中发生物理变化的是( )
A . 光合作用
B . 食物消化
C . 瓷碗破碎
D . 氢氧化钠放置在空气中变质
-
-
3.
分类是化学研究常用的方法.下列对物质分类正确的是( )
A . 氧气(O2)和水(H2O)都属于氧化物
B . 氧气(O2)和臭氧(O3)都属于单质
C . 碳酸钙(CaCO3)和甲烷(CH4)都属于有机物
D . 火碱(NaOH)和纯碱(Na2CO3)都属于碱
-
4.
今年央视3.15晚会曝光,少数不法厂家向液化石油气中掺入了二甲醚(C2H6O),二甲醚会对液化气罐的配件造成腐蚀,存在安全隐患.下列关于二甲醚的说法错误的是( )
A . 属于氧化物
B . 每个分子中含有9个原子
C . 碳、氢、氧元素的质量比为12:3:8
D . 碳元素的质量分数约为52.2%
-
5.
如图所示是某反应前后的微观示意图,“○”和“●”表示两种不同的原子.则该反应( )
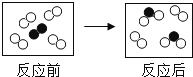
A . 是化合反应
B . 有单质生成
C . 反应前后分子种类不变
D . 参加反应的两种分子个数比为4:1
-
6.
下列各组物质在溶液中不发生化学反应而能共存的是( )
A . MgCl2、AgNO3、KNO3、HCl
B . H2SO4、BaCl2、Na2SO4、NaOH
C . Na2SO4、KNO3、Na2CO3、NaCl
D . NH4HCO3、NaOH、HCl、NaCl
-
7.
向AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,充分反应后再加入稀盐酸无明显现象.下列说法正确的是( )
A . 一定有锌粉剩余
B . 所得溶液中一定有Zn2+、Cu2+
C . 一定有银粉生成
D . 所得溶液中一定有Cu2+、Ag+
-
-
9.
下列实验的实验现象与实验结论都正确的是( )
| 实验操作 | 实验现象 | 实验结论 |
A | 将一根未打磨的铝条放入 硫酸铜溶液中 | 无紫红色固体析出 | 铝不如铜活泼 |
B | 将带火星的木条伸入氧气中 | 木条复燃 | 氧气能支持燃烧 |
C | 将CO通过灼热的氧化铜 | 黑色氧化铜变成红色 | CO具有可燃性 |
D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应放热 |
A . A
B . B
C . C
D . D
-
10.
阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用.下列关于该阻燃剂防火原因的叙述中错误的是( )
A . 反应吸热,降低了可燃物的着火点
B . 生成氧化铝覆盖在可燃物表面,隔绝空气
C . 生成大量水蒸气,降低可燃物周围氧气浓度
D . 反应能够降低温度,可燃物不易达到着火点
二、<b >选择题(每小题</b><b >2</b><b>分,共</b><b>10</b><b >分,每题有</b><b >1-2</b><b>个符合题意)</b><b>.</b>
-
11.
下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
A . 紫色石蕊试液
B . 氯化钠溶液
C . 铜粉
D . 氧化铜粉末
-
12.
分析推理是化学学习中常用的思维方法.下列说法正确的是( )
A . 酸性溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的溶液一定呈酸性
B . 溶液具有均一、稳定的特征,所以均一、稳定的物质一定是溶液
C . 单质是由同种元素组成的,但同种元素组成的物质不一定是单质
D . 复分解反应中有沉淀、气体或水生成,所以有上述物质生成的反应就是复分解反应
-
13.
为除去下列物质中的杂质(括号内是杂质),下列操作方法正确的是( )
选项 | 物质 | 操作方法 |
A | N2(O2) | 燃烧硫粉 |
B | CaO粉末(CaCO3) | 加足量的水,充分搅拌后过滤 |
C | NaOH溶液(Ca(OH)2) | 通入过量CO2气体,充分反应后过滤 |
D | CuSO4溶液(H2SO4) | 加入过量CuO粉末,加热,充分反应后过滤 |
A . A
B . B
C . C
D . D
-
14.
下列说法正确的是( )
A . 生成盐和水的反应不一定是中和反应
B . 有单质和化合物参加的反应一定为置换反应
C . 两种化合物反应,生成另两种化合物的反应一定是复分解反应
D . 分解反应的反应物一定是化合物
-
15.
将一定量的乙醇(C
2H
6O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
下列判断正确的是( )
A . 表中a的值为2.6
B . X一定是该反应的催化剂
C . X可能含有氢元素
D . 若起始时氧气的质量是9.6g,则无X生成
三、<b >填空题(本大题共</b><b >5</b><b>小题,共</b><b>20</b><b >分)</b>
-
16.
选择与下列用途相对应的物质的化学式填空A.甲烷 B.盐酸 C.碳酸钠 D.氢氧化钙 E.氢气 F.干冰
①用于改良酸性土壤
②密度最小的气体,最清洁的高能燃料
③最简单的有机物
④人体胃液的成分
⑤用于玻璃、造纸、纺织、洗涤剂
⑥用于制冷剂,人工降雨.
-
17.
紫薯营养丰富,具有特殊的保健功能,紫薯中富含淀粉、蛋白质、维生素A、维生素B、维生素C、锌、铁、钙、硒等.
①紫薯中维生素(选填“A”、“B”或“C”)可预防坏血病;
②紫薯中还缺乏一种能给人体供能的营养素是.
-
18.
俄国化学家门捷列夫在总结前人经验的基础上,通过艰辛的努力,终于提出了现代元素周期表的雏形.下表为元素周期表的部分元素的相关信息,利用下表回答相关问题: 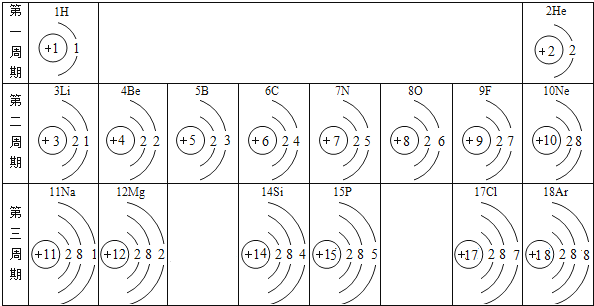
-
(1)
请画出16号元素原子结构示意图,化学反应中该原子比较容易(填“得到”或“失去”)电子变成离子;
-
(2)
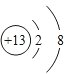 表示的是(填离子符号);
表示的是(填离子符号);
-
(3)
上表中活泼的金属元素与地壳中含量最多的元素组成的化合物是(填化学式,任意填写一种).
-
19.
能源、环境与人类的生活和社会发展密切相关.
-
(1)
目前,人类以化石燃料为主要能源,常见的化石燃料包括煤、石油和.
-
(2)
为减少污染,提高煤的利用率,可将其转化为可燃性气体,此过程可以认为是碳与水的反应,其微观示意图如下所示: 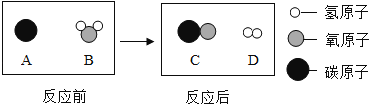
①该反应的基本反应类型为;
②该反应生成物的分子个数比为;
-
(3)
为减少温室气体排放,人们积极寻找不含碳元素的燃料,经研究翻新NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景.
①NH3中氮元素和氢元素的质量比为;
②将NH3燃烧反应的化学方程式补充完整:4NH3+3O2 6H2O+
6H2O+
-
(4)
软玉也称中国玉,以新疆“和田玉”为代表,生成和田玉矿床的反应方程式为5CaMg(CO3)2+8SiO2+X  CaMg(Si4O11)2(OH)+7CO2+3CaCO3 , 则X的化学方程式为.
CaMg(Si4O11)2(OH)+7CO2+3CaCO3 , 则X的化学方程式为.
-
20.
由Mg(OH)2和MgO组成的混合物,测得其中含镁元素的质量分数为48%.取该混合物10g,将其投入适量的稀硫酸中恰好完全反应,所得溶液中溶质的质量为.
四、<b >简答题(本大题共</b><b >5</b><b>题,共</b><b>23</b><b >分)</b>
-
-
22.
如图是甲、乙两种固体物质的溶解度曲线.
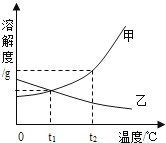
-
-
(2)
t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲乙(填“>”、“<”或“=”).
-
(3)
把甲物质的不饱和溶液变为饱和溶液,下列有关说法正确的是
(填序号,下同)
a.溶剂的质量一定变小 b.溶质的质量可能不变
c.溶质的质量分数一定变大 d.溶液的质量一定变大
e.该饱和溶液还可以溶解其它物质
-
(4)
通常情况下,在实验室用固体甲配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平(带砝码盒)、烧杯和
.
a.酒精灯 b.药匙 c.玻璃棒 d.漏斗 e.铁架台 f.量筒 g 胶头滴管.
-
23.
将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题:
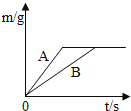
-
-
(2)
对于该图象的理解,下列说法正确的是
(填序号).
①A表示锌和稀硫酸的反应曲线
②反应结束后两种金属一定都有剩余
③反应结束后稀硫酸都没有剩余
④反应结束后消耗两种金属的质量相等
⑤反应结束后所得溶液质量相等.
-
24.
在盐酸、碳酸钠、火碱、二氧化碳、镁、食盐、石灰水、氧化剂、银、木炭粉等物质中,按类别选择适当物质,使如图连线的物质之间能相互反应,并回答问题:
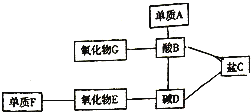
-
-
-
-
-
25.
根据表中五种气体在标准状况下的密度和溶解性,回答下列问题:
| 空气 | NH3 | CH4 | HCl | O2 |
密度/gL﹣1 | 1.293 | 0.771 | 0.717 | 1.629 | 1.43 |
溶解性 | ﹣﹣ | 极易溶 | 难溶 | 极易溶 | 难溶 |

-
(1)
既能用排水法,又能用向上排空气法收集的气体是.
-
(2)
用如图所示盛满水的集气瓶收集CH4 , 气体应从端进入.
五、<b >实验题(本大题共</b><b >2</b><b>题,共</b><b>17</b><b >分)</b>
-
26.
根据下列装置,结合所学化学知识回答下列问题. 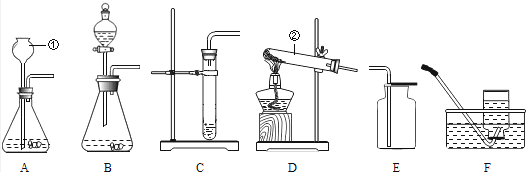
-
-
(2)
实验室制取少量二氧化碳时,发生装置最好选用,收集装置选用;如需随时控制生产气体的量并节约药品,发生装置最好选用.(填编号)
-
(3)
实验室用高锰酸钾制取氧气时,发生装置应选用(填编号);写出其反应的化学方程式.
-
(4)
如用E装置收集O2 , 检验O2是否收集满的方法是.
-
27.
某粗盐样品中含有杂质氯化镁、氯化钙.某同学设计了以下提纯方案: 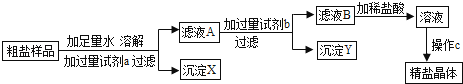
请回答下列问题:
-
(1)
方案中加入过量试剂a若为氢氧化钠溶液,则其目的是为了除去粗盐中的.
-
(2)
在过滤操作中,除用到带铁圈的铁架台、烧杯、玻璃棒外,还需要用到的仪器是.
-
-
(4)
向滤液B滴加稀盐酸的过程中,当观察到的溶液的现象为时,应停止滴加,如果滴加的稀盐酸过量,对最后得到的精盐晶体的成分(填“有”或“没有”)影响.
-
-
(6)
工业上用电解饱和食盐水的方法可制取氢氧化钠、氢气、和氯气,写出反应的化学方程式.
六、<b >计算题(本大题共</b><b >2</b><b>小题,共</b><b>10</b><b >分)</b>
-
28.
酒精的化学式为C
2H
5OH.计算:
①酒精的相对分子质量为;
②酒精中C、H、O三种元素的质量比是;
③23克酒精中含氧元素的质量是g.
-
29.
称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示.试回答下列问题:(提示:BaCl2+Na2SO4═BaSO4+↓+2NaCl) 
-
-
(2)
恰好完全反应时消耗Na2SO4溶液的质量是g.
-
(3)
恰好完全反应时所得溶液中溶质的质量分数是多少?(精确到0.1%)

![]() 6H2O+
6H2O+![]() CaMg(Si4O11)2(OH)+7CO2+3CaCO3 , 则X的化学方程式为.
CaMg(Si4O11)2(OH)+7CO2+3CaCO3 , 则X的化学方程式为.