

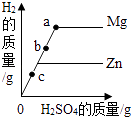
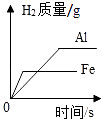
 等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应
B .
等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应
B . 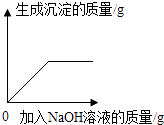 向H2SO4和MgSO4的混合溶液中滴加NaOH溶液
C .
向H2SO4和MgSO4的混合溶液中滴加NaOH溶液
C .  向pH=13的氢氧化钠溶液中不断加水稀释
D .
向pH=13的氢氧化钠溶液中不断加水稀释
D . 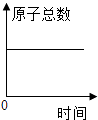 化学反应中,原子总数随时间的变化
化学反应中,原子总数随时间的变化
实验一:
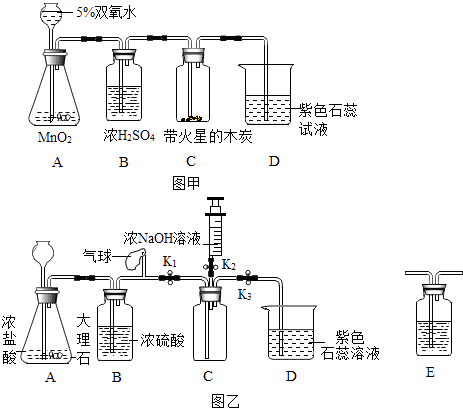
同学们利用如图乙装置验证CO2能与NaOH反应.(装置气密性良好)
(1 )打开K1、K3 , 关闭K2 , 当D中液体变红色时,可确定C中.
(2 )C中收集满CO2后,关闭K1 , 打开K2 , 将注射器中5mL浓NaOH溶液推入C中,观察到D中液体流入C中,说明CO2与NaOH发生了反应.
①同学们发现此装置有明显不足,认为应该在(填装置字母序号)之间增加洗气瓶E,其作用是.
②继续完善实验,还应补充一个对比实验,即将C装置中的浓NaOH溶液改为.
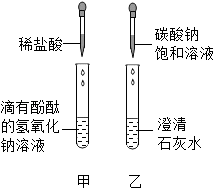
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和(写物质名称).
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是.(写一种猜想)
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | ①有白色沉淀,溶液呈红色. | 的猜想正确. |
②. | 的猜想正确. | |
③. | 的猜想正确. |