①塑料属于(填字母序号).
a.合成材料 b.复合材料 c.金属材料
②建筑外墙的复合保温材料采用铝合金锁边,金属铝耐腐蚀是因为.
①化石燃料包括、石油、天然气,石油综合利用大大的提高了其利用价值,石油的分馏属于变化(填“物理”或“化学”).
②出行使用电动自行车,有利于减少环境污染,电动自行车行驶时电池将能转化为电能.
①若要检测某河水是否显酸性,可选用(填字母序号).
a.石蕊试液 b.pH试纸 c.酚酞试液 d.碳酸钙
②下列做法会造成水体污染的是(填字母序号).
a.随意弃置废旧电池 b.严格监管化肥和农药的使用
c.工业废水经处理达标后再排放 d.含二氧化硫、二氧化氮工业废气任意排放
③生活中常用的方法,即可降低水的硬度.
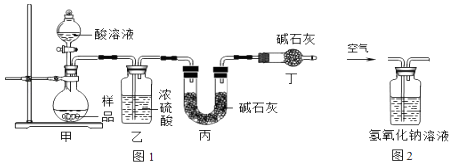
Ⅰ.A组同学设计了如图1的实验装置.
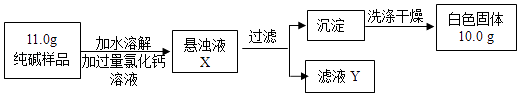
(1 )滤液Y中含有的溶质有(填写化学式).
(2 )证明CaCl2已过量的方法是(填写字母序号),然后观察现象判断.
A.静置悬浊液X,向上层清液中继续滴加少量氯化钙溶液
B.取少量滤液Y于试管中,滴加氯化钙溶液
(3 )如果沉淀没有洗涤操作会造成碳酸钠质量分数(填“偏大”或“偏小”或“无影响”).
(4 )通过以上提供的数据计算出样品中碳酸钠的质量分数为.(写出计算过程,结果保留至0.1%)