某化学小组为验证甲烷的组成,设计了如图所示实验. 该实验装置气密性良好,实验中所用试剂均足量.
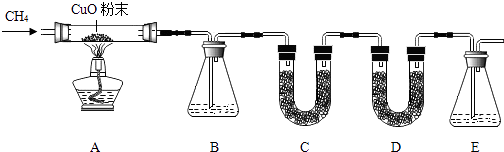
已知装置 B、C、D、E中分别盛有浓硫酸、白色无水CuSO4固体、碱石灰、澄清石灰水,而且已知白色无水CuSO4固体遇水会变蓝色.
(1 )实验步骤:
Ⅰ.通人甲烷气体.
Ⅱ.点燃酒精灯加热,反应一段时间后,停止加热.
Ⅲ.继续通甲烷至玻璃管冷却.
(2 )有关现象:
①A中黑色固体变红色;②C中未见变蓝色;③E中未见出现浑浊.
(3 )有关数据:
A中玻璃管及物质总质量/g | B装置及物质总质量/g | D装置及物质总质量/g | |
反应前 | 108.0 | 212.0 | 131.0 |
反应后 | 106.4 | 212.9 | 132.1 |
请回答下列问题: