
【猜想与假设】猜想1:在常温下不能反应,在加热条件下也不能反应;
猜想2:在常温下不能反应,在加热条件下能反应。
【实验与现象】步骤1:将一小块铜片放入试管中,加入足量的浓硫酸,无明显现象;
步骤2:加热该试管,铜片上有气泡生成,并闻到刺激性气味;
步骤3:检验产生的有刺激性气味的气体;
步骤4:立即停止加热;
步骤5:将试管中的残液慢慢倒入少量水中,溶液呈蓝色。
Ⅱ:经检验产生的气体是SO2 , 立即停止加热可避免产生更多的SO2;
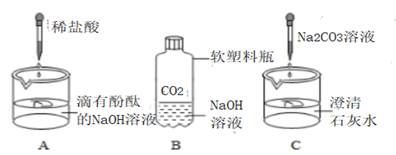
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有氯化钠。
老师问:废液中还可能有什么物质?
某同学脱口而出:废液中一定含有氢氧化钠,他的说法正确吗?同学们认为不准确,理由是:。
请你写出在原实验的基础上作出进一步判断的方法:。
①下列化肥中,属于氮肥的是。(填字母)
A.碳酸氢铵(NH4HCO3) B.草木灰(主要成分K2CO3) C.磷矿粉[Ca3(PO4)2]
②草木灰呈碱性,不能与选用的氮肥混合施用,理由是。
①目的是促进绿色植物的光合作用。
②若提供的气体肥料CO2中混有少量的SO2 , 为了除去SO2 , 现设计以下两种方法:
甲方法:将气体通过足量的碳酸氢钠溶液;乙方法:将气体通过足量的氢氧化钠溶液。
【提供资料】
Ⅰ.CO2与NaHCO3不会发生反应
Ⅱ.SO2+2NaHCO3==Na2SO3+H2O+2CO2
Ⅲ.SO2+2NaOH==Na2SO3+H2O
请你利用提供的资料和所学的知识分析:选择上述甲方法的理由是。