 B .
B .  C .
C .  D .
D . 
①写出符合要求的物质化学式:
自然界中最硬的物质是,空气中最稳定的气体是。
②生活中某化学反应的微观过程如图,其中“ ![]() ”和“
”和“ ![]() ”表示两种不同原子。
”表示两种不同原子。
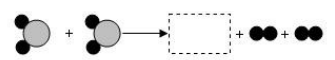
该反应属于反应(填基本反应类型)。虚线框内应填的微观图示是(选填编号),推断的依据是。
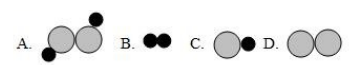
①日常生活中人们常把煤做成蜂窝状(如下图),这样做的目的是。

②共享单车轮胎材料含甲苯二异氰酸酯,化学式为C9H6N2O2 , 它由种元素组成,摩尔质量为,87g甲苯二异氰酸酯的物质的量是mol,1mol甲苯二异氰酸酯分子约含个氧原子。
①碳酸饮料中,二氧化碳与水反应的化学方程式是。
②洪涝地区的灾民将河水转化为可饮用水,以下处理顺序合理的是。
①化学沉降(用明矾) ②消毒杀菌 ③自然沉降 ④加热煮沸
A.③②①④
B.③①②④
C.③①④②
D.①③④②
|
温度 |
1 |
20 |
40 |
60 |
70 |
80 |
|
S(KNO3) |
13.3 |
31.6 |
63.9 |
110 |
100 |
169 |
①分析上述数据,某温度时的硝酸钾溶解度数据可能存在较大的误差,该温度是℃;
请根据表中的数据,在坐标图中描点、绘制符合硝酸钾溶解度变化规律的曲线。
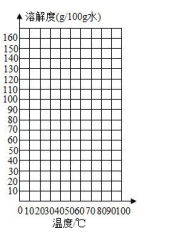
②60℃时,50g水中最多溶解gKNO3。
③除去KNO3晶体中混有的少量NaCl,通过:溶解、蒸发浓缩、、、洗涤、干燥得到比较纯净的KNO3晶体。
④将硝酸钾的饱和溶液变为不饱和溶液,说法正确的是(选填编号)。
A.溶解度一定不变
B.溶剂质量一定增大
C.溶质质量一定不变
D.溶质质量分数一定减小
⑤20℃时,实验室配制一瓶最浓的硝酸钾溶液。在配制过程中操作顺序是(填编号),溶质质量分数为(精确0.1%),装瓶后贴上标签并写上。
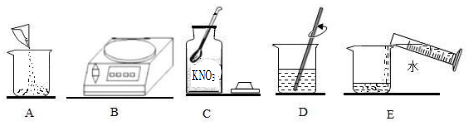
⑥取上述⑤配制的20℃100g硝酸钾的饱和溶液(如A烧杯)进行如下操作,请回答:
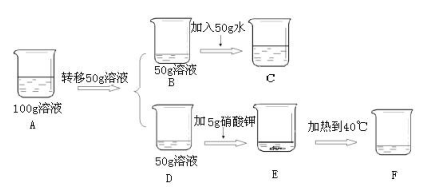
上述溶液中一定是不饱和溶液的是(填“A、B、C、D、E、F”),所含溶质的质量BF(填“>”、“<”或“=”,下同),其中A、C、E、F溶液的溶质质量分数的大小关系是。
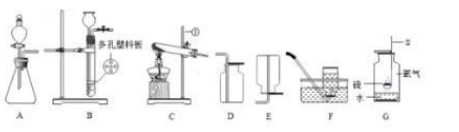
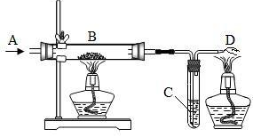
①根据要求完成下表。
| 序号 | 探究实验 | 简答 |
| I | 若为H2与CuO的反应 | B处玻璃管中的现象是; B处反应的化学方程式; |
| II | 若为CO与CuO的反应 | C处反应的化学方程式; D处酒精灯点燃的目的。 |
| III | 若为CO2与C的反应 (B处换成酒精喷灯) | C处澄清石灰水的作用; D处酒精灯点燃的目的。 |
②实验I通过B处的现象已能确定铜的生成,确定另一产物水生成的方法是B与C之间加装一个装有(填药品名称)的干燥管。
③对实验II分析错误的是(选填编号)。
a.反应开始后通入0.1mol一氧化碳可生成0.1mol铜
b.B中固体减少的质量小于C中增加的质量
c.实验结束时应先熄灭B处酒精灯
d.反应结束后继续通入一氧化碳的目的是防止铜被氧化