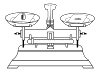
 称量氯化钠
B .
称量氯化钠
B . 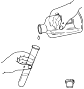 倾倒液体
C .
倾倒液体
C . 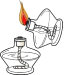 点燃酒精灯
D .
点燃酒精灯
D . 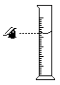 读取液体体积
读取液体体积
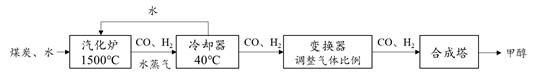

农药在农业生产中发挥着至关重要的作用,可以有效地防控农作物病虫害。但某些地区确实出现过农药残留超标事件,让一些人“谈药色变”。怎样科学地减少果蔬中的农药残留呢?有些农药随着温度的升高,分解会加快。通过在沸水中焯或使用蒸、炒等烹饪手段可以去除蔬菜中氨基甲酸酯类农药的残留。部分农药在空气中能够缓慢地分解为对人体无害的物质。所以对一些易于保存的农产品,如胡萝卜、南瓜、土豆等,可以在室外存放一定时间来减少农药残留量。有科研人员监测了番茄中三唑酮(C14H16ClN3O2)在温室大棚内和室外的分解规律,如图。

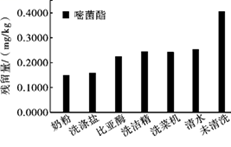
去皮可以有效减少果蔬中的农药残留。但部分果蔬不容易去皮,如生菜、草莓、樱桃等,因此清洗成为了消费者去除农药残留的重要方式。由于大多数农药难溶于水,可利用洗菜机或加入洗涤盐等方式提高农药残留的去除效果,有人研究了利用不同方法去除黄瓜中嘧菌酯农药残留的效果,如图所示。
可见,减少农药残留的关键是认识物质的性质。基于农药的不同性质,采用有针对性的方法来去除。
依据文章内容回答下列问题。

(查阅资料)氮气密度略小于空气;压强不变时,气体温度越低,密度越大。
实验1:探究氮气能否用来灭火(所用容器均为隔热材料,下同)
|
实验编号 |
1-1 |
1-2 |
1-3 |
|
实验内容 |
| | |
| 实验现象 | 蜡烛持续燃烧 | 蜡烛缓慢熄灭 | 蜡烛熄灭 |
实验2:探究灭火与氮气含量是否有关
|
实验编号 |
2-1 |
2-2 |
2-3 |
|
实验内容 |
| | |
| 实验现象 | 蜡烛没有熄灭 | 蜡烛缓慢熄灭 |