①若要验证小莹同学的猜想:可向反应后的溶液中加入金属,结果发现在该金属表面只生成红色固体,则证明该同学的猜想是错误的.
②因为稀盐酸是新配制的,不存在变质的可能,所以小斌同学的猜想也是错误的.
③小歆为了验证自己的猜想是正确的,在不改变药品和实验方法前提下,向实验结束后的试管中加入某种物质适量,结果发现溶液呈现蓝色.小歆加入的是下列哪种物质
A.酒精 B.水 C.硫酸铜溶液 D.氯化铜溶液
爱动脑筋的小歆对这一实验做了一点改进,将一根铜丝擦光亮后,一端绕成螺旋状放在酒精灯火焰上灼烧至表面出现黑色,然后趁热放进稀盐酸中,一会儿就可以看到螺旋上的,溶液也由无色变成蓝色.化学方程式
【提出猜想】从物质组成元素的角度分析,放出的气体可能是SO2、O2、H2 .
【查阅资料】SO2易溶于水,它能与NaOH反应,生成Na2SO3 .
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
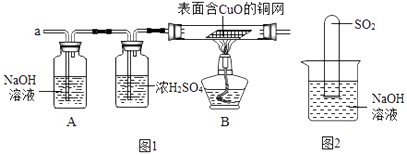
①甲同学认为是O2 , 收集一瓶该气体,检验方法是.
②乙同学认为是SO2 , 则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量.写出SO2与NaOH反应的化学方程式.
③实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.如果放出的是O2和H2 , 你认为方案中的安全隐患是.
结论:铁粉与硫酸铜溶液反应时,产生的气体是.
①由上述实验可以推出,硫酸铜溶液中可能含有(选填:“酸性”、“碱性”或“中性”)物质.
②不通过称量,如何判断SO2与NaOH溶液发生了反应呢?有一同学设计了图2所示的装置进行实验,发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是.要得到科学严谨的结论,仍利用该装置,补做的实验是
【提出问题Ⅰ】固体酒精是固态的酒精吗?
【查阅资料Ⅰ】酒精,学名乙醇,化学式为C2H6O,熔点为﹣114.1℃,沸点为78.5℃,易溶于水,能与水以任意比互溶.
【实验探究Ⅰ】取少量固体酒精置于蒸发皿中,用火柴点燃,固体酒精完全燃烧后,蒸发皿中残留了少量白色固体.
【提出问题Ⅱ】白色固体是什么呢?
【查阅资料Ⅱ】以硬脂酸和氢氧化钠反应生成的硬脂酸钠作为凝固剂,将酒精填充在硬脂酸钠骨架间隙中,即可得到固体酒精.固体酒精在较高温度下燃烧时,硬脂酸钠可完全转化为硬脂酸和氢氧化钠,硬脂酸和酒精均可完全燃烧生成二氧化碳和水.
【实验探究Ⅱ】验证白色固体的成分.回答下列问题:
实验操作步骤 | 实验现象 | 实验结论 |
①; ②. | ①; ②. | 白色固体是NaOH和Na2CO3的混合物 |
方案I:硫化铜在硫杆菌的作用下跟空气中的氧气发生反应,生成硫酸铜,反应方程式为:CuS+2O2 CuSO4;
方案Ⅱ:高温煅烧硫化铜,生成氧化铜;氧化铜跟硫酸反碰生成硫酸铜.根据上述信息,请你回答:
方案一:固体混合物 溶液
固体
方案二:固体混合物 溶液
固体
你认为合理的实验方案是.
说明另一方案不合理的理由:.