“菠菜豆腐”是我国的传统菜肴,近年来,有关“菠菜豆腐”的争论主要集中在钙吸收率方面。菠菜中富含易溶于水的草酸,若单独吃菠菜,其中的草酸会结合胃内食糜中的部分铁和锌,还能够进入血液,沉淀血液中所含的钙。而将豆腐与菠菜同食,豆腐中的可溶性钙与菠菜中的草酸结合成不溶性的草酸钙(CaC2O4)沉淀,既能够保护食物中的铁和锌等元素,还能保证人体内的钙不被草酸结合。因此,豆腐与菠菜同食仍不失为一个好的搭配。
研究人员以新鲜菠菜和新鲜豆腐为材料,进行了“菠菜豆腐”烹调方法的研究。
(实验1)探究菠菜质量对菜肴中可溶性钙含量的影响。实验结果如下:
豆腐/ g | 10 | 10 | 10 | 10 | 10 |
菠菜/ g | 5 | 10 | 15 | 20 | 25 |
可溶性钙/总钙 | 0.364 | 0.287 | 0.186 | 0.125 | 0.088 |
(实验2)探究菠菜焯水时间对菜肴中可溶性钙含量的影响。
用100g豆腐和250g菠菜(焯水时间不同)制成菜肴,测定每100g“菠菜豆腐”中可溶性钙的质量,结果见下图。
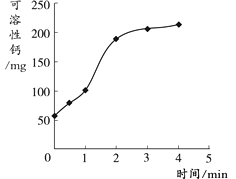
以上研究表明,烹调“菠菜豆腐”时,如能适当减少菠菜的比例,并预先将菠菜焯水,则豆腐中钙的吸收率将会显著提高。
根据文章内容,回答下列问题:
①查阅资料:白色粉末的主要成分是过碳酸钠(Na2CO4),常温下与水反应生成氧气。
②用一定溶质质量分数的NaOH和Na2CO3两种溶液进行如下实验。
NaOH溶液 | Na2CO3溶液 | |
滴加酚酞溶液 | 溶液变红色 | 溶液变红色 |
加入稀盐酸 | 无明显现象 | 现象Ⅰ |
加入澄清石灰水 | 无明显现象 | 现象Ⅱ |
加入 1%的CaCl2溶液 | 溶液变浑浊 | 溶液变浑浊 |
加入 0.1%的CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
表中的现象Ⅰ为,现象Ⅱ对应的化学反应方程式为。
实验1:检验气体
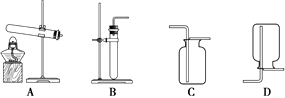
小明用白色粉末和水反应制取并收集产生的气体时,应选用的装置是(填序号)。 经检验该气体是氧气。
实验2:检验反应后溶液中的溶质成分
【猜想假设】小明猜想:Na2CO3 小刚猜想:Na2CO3和NaOH
【进行实验】小明取实验1反应后的溶液于试管中,滴加1%的CaCl2溶液,观察到有白色沉淀生成,认为自己的猜想正确。
【表达交流】①小刚对小明的实验方案提出质疑,他的理由是。
②为了证明小明的猜想是否正确,你的实验方案是。
根据上述探究可知,保存该白色粉末时应注意。
实验装置 | 实验1 | 实验2 |
| Ⅰ. A中盛有水,液面浸没下端导管口,B中盛有含酚酞的NaOH溶液 Ⅱ.将注射器中的浓硫酸注入A中,并保持注射器活塞不动,充分接触后,打开K1和K2 | Ⅰ. A中充满CO2 , B中盛有一定量的水 Ⅱ. 将注射器中的NaOH溶液(足量)注入A中,充分反应后,打开K1和K2 |