为了解铬在金属活动性顺序中的相对位置关系,彬彬和同学们选择金属铜和铝进行实验探究。
【查阅资料】
资料1:铬是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。
资料2:铬在发生置换反应时生成Cr2+ , 含有Cr2+的溶液常显蓝色。【实验药品】铝片、铬片、铜片、稀硫酸、稀盐酸、CrSO4溶液。
【实验过程】
试管 1 | 试管 2 | 试管 3 | |
实验现象 | 金属片表面产生气泡缓慢,溶液逐渐变蓝色。 | 金属片表面产生气泡较快。 | |
实验结论 | 三种金属的金属活动性由强到弱的顺序为. | ||
写出试管1中发生反应的化学方程式.
彬彬同学了解到某电镀厂的废水中含有AgNO3、Cu(NO3)2和Cr(NO3)2 , 为了从中回收贵重金属银和硝酸铬晶体,他设计了如下实验流程
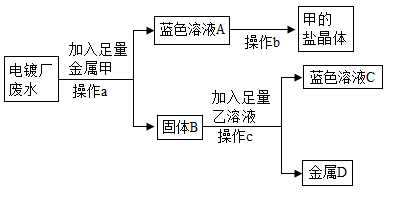
分离溶液A和固体B 时,需要使用玻璃棒,玻璃棒在此操作中所起的作用是。加入乙溶液时反应的化学方程式为(写一个)。反应前固体B质量(填“大于”、“小于”或“等于”)反应后固体D的质量。