 +3SnCl4+4 H2O
+3SnCl4+4 H2O 已知:苯胺类似氨气有碱性,与盐酸反应生成可溶于水的盐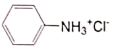 ;部分物质物理性质见下表:
;部分物质物理性质见下表:
| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/ |
| 苯胺 | | 184 | 微溶于水,易溶于乙醚 | 1.02 |
| 硝基苯 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
| 乙醚 | | 34.6 | 微溶于水 | 0.7134 |
回答下列问题:
步骤ⅰ.将碱化液蒸馏,收集到苯胺与水的混合物,分液得粗苯胺和水溶液;
步骤ⅱ.步骤ⅰ所得水溶液中加至饱和,用乙醚萃取得萃取液与粗苯胺合并:
步骤ⅲ。合并溶液用干燥剂干燥,过滤,将滤液蒸馏并收集温度时的馏分得到苯胺。
①步骤ⅰ蒸馏不需温度计控制温度,试依据收集馏分的特点,分析原因是。
②步骤ⅱ萃取分液操作过程中要远离明火及热源,原因是。如果没有步骤ⅱ,苯胺的产率(填“不变”、“增大”或“减小”)。步骤ⅲ中干燥剂可以选用(填序号)
a.浓硫酸 b.五氧化二磷 c.固体
③步骤ⅲ中蒸馏获得苯胺的温度的范围为。
苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:
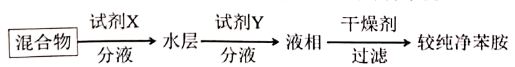
试剂是,试剂
是,“液相”是(填“水层”或“有机层”)