臭氧的化学式是O3 , 在通常状况下是淡蓝色、有鱼腥臭味的气体。在常温常压下,臭氧稳定性较差,久置后可自行转化为氧气,并放出热量。
若将O2通过臭氧发生器,在无声放电条件下,O2可以转化为O3.如图为臭氧转化为氧气的微观示意图:
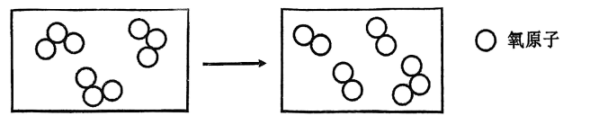
在离地面25千米处有一个厚度极薄的臭氧层。臭氧层能吸收太阳辐射的大量紫外线,使地球上的生物免遭紫外线的伤害。但是,一旦臭氧到了距离地面10-100米左右的近地面层,就换了一副可怕面孔,变成了“健康杀手”。臭氧浓度超标对人体的伤害表现在会引起咽喉肿痛、胸闷咳嗽、头晕等不适反应。所以,有句话形容臭氧再合适不过—在天成佛、在地成魔。


请回答以下问题:
A 液面高于滤纸边缘 B.滤纸没有紧贴漏斗内壁而留有气泡
C.滤纸破损 D.漏斗下端没有紧贴烧杯内壁

a.分子大小 b.分子种类 c.分子间间隔

宏观变化 | 微观解释 |
|
|
|
|

查阅资料:大部分金属氧化物与稀盐酸(主要成分是HCl)反应能生成对应的氯化物和水。如: ,
①氧化钇(Y2O3)中,Y元素的化合价为。
②“酸溶”过程中,氧化钇与盐酸反应的化学方程式是。
③碳酸钇加热灼烧分解还会生成二氧化碳,该反应的化学方程式是。
①用化学用语表示:SbCl3中含有的阳离子,锑酸。
②Sb2O5是一种重要的阻燃剂,Sb2O5读作。
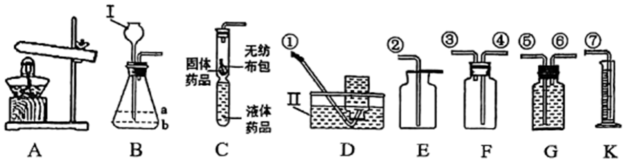

关于上述探究实验,下列说法正确的是____(填标号)。
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集O2平均速率mL。min-1 |
实验1 | 0.49 | 无 | 0 | 11.8 |
实验2 | 0.49 | MnO2 | 0.2 | 28.2 |
实验3 | 0.49 | 碗渣粉(60目) | 0.2 | 49.1 |
实验4 | 0.49 | 碗渣粉(30目) | 0.2 | 23.7 |
实验5 | 0.49 | 红砖粉(60目) | 0.2 | 28.3 |
实验6 | 0.49 | 红砖粉(30目) | 0.2 | x |
A.10.6 B.21.1 C.23.8 D.49.1