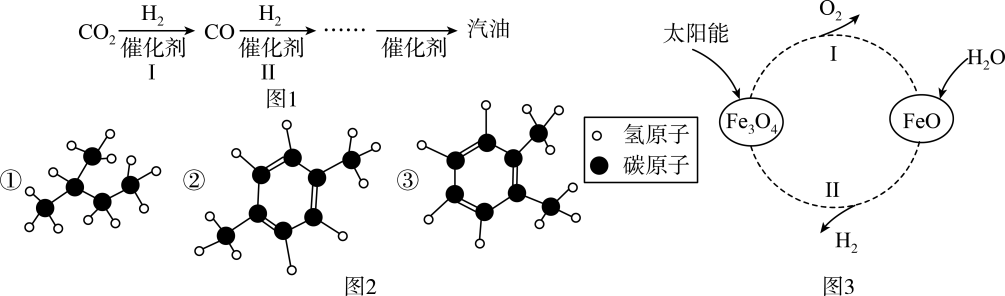
中科院科学家研发出新型催化剂,成功实现了二氧化碳直接加氢制取汽油。简要流程如图1所示,制得汽油中部分成分分子的结构如图2所示,所需H2可通过图3所示过程获得。
元素名称 | 硅 | 磷 | 硫 | 氯 |
原子结构 示意图 |
|
|
|
|
①上表中x=,氯原子得到一个电子所形成离子的离子符号是。
②从原子结构上分析,表中元素在元素周期表中均位于第三周期的原因是。
③含上表中某元素的一种化合物能与氢氧化钠发生中和反应生成Na2SO4 , 该化合物为·(填化学式)。

①物质X的一个分子中含有10个原子,则其化学式。
②写出五氧化二磷与水反应生成磷酸(H3PO4)的化学方程式:。
③磷酸二氢钾(KH2PO4)可用于改良碱性土壤,它与物质(填“Y”或“Z”)所含磷元素的化合价相同。
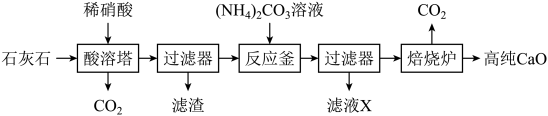
已知:石灰石主要成分为碳酸钙,含有少量不溶于水和酸的二氧化硅。硝酸(HNO3)具有挥发性,受热易分解。通常状况下,1体积水中能溶解约700体积的NH3或约1体积的CO2
书中提到有关墨的制作方法:凡墨,烧烟漫质而为之。松木不完全燃烧形成烟(主要成分为炭黑),在烟中加入天然胶等可制得墨。
古代用墨书写的字画长久不褪色,原因是墨汁中的炭黑。书中记载:泥固塞其孔,然后使水转釉。是指高温下CO将红砖中的Fe2O3转化为Fe3O4而形成青砖,该转化的化学方程式为。
“燔石”篇中介绍了白矾(指明矾)净水的技术。明矾[KAl(SO4)2·12H2O]加入水中可以得到氢氧化铝胶体,该变化属于(填“物理”或“化学”)变化。现将此法制得的胶体装入半透膜内,并将此半透膜浸入盛有蒸馏水的烧杯中;一段时间后取烧杯中液体少量,滴入溶液,产生白色沉淀,证明能透过半透膜。

①取水过程中,活性炭可除去水中的异味,这是因为活性炭具有。
②RO反渗透膜能截留水中细菌、病毒,还可除去其中的(填离子符号)等多种金属离子,从而降低水的硬度。
【查阅资料】①“发热包”主要由生石灰、铁粉、镁粉、铝粉、活性炭、氯化钠组成;
②铝粉与强酸、强碱溶液都能迅速反应生成氢气,同时放出大量热。
I、探究发热包的发热原理
【实验探究1】

测得实验开始后600s内瓶中温度均呈上升趋势。实验所用试剂X的组成及部分数据如下表:
实验 序号 | 试剂X的组成 | 600s时的温度/C | |
活性炭粉g | 食盐g | ||
① | 6 | 3 | 35.1 |
② | 6 | 0 | 27.9 |
③ | 0 | 3 | 23.3 |
④ | 0 | 0 | 21.1 |
【实验分析2】
能证明活性炭粉可加快铁锈蚀的实验组合有(填实验序号)。
【实验探究3】
兴趣小组通过如下实验研究发热包的成分:
步骤1取少量发热包中固体于试管中,加水振荡,静置,滴入几滴酚酞溶液,溶液变为红色。
步骤2另取少量发热包中固体于试管中,逐渐加入稀盐酸至不再产生气泡为止,反应停止后有黑色固体剩余,溶液呈浅绿色。
步骤3取步骤2所得上层清液少许于另一试管,滴加硝酸银溶液,有白色沉淀生成,继续滴加稀硝酸,沉淀不溶解。
【实验分析3】
“步骤2”中最终溶液呈浅绿色是因为(用化学方程式表示)。
请另行设计实验证明该发热包中含有铝粉。简述实验过程(包括操作和现象):(除发热包外可供选择的试剂有稀盐酸、NaOH溶液、AgNO3溶液)。
使用图3所示自热米饭时,在外盒中禁用热水,若不小心加入热水,可能会使餐盒炸裂,请从微观角度分析餐盒炸裂的原因:。
