A.金 B. 铜 C. 汞 D. 钨
①原料锡砂中的SnO2和木炭反应得到锡和二氧化碳,化学方程式为。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是。

①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是。
②已知锌的沸点为907℃。泥罐下部温度可达1200℃,上部约为600℃,该工艺从反应混合物中收集液态锌的方法属于(填标号)。
A.结晶 B.蒸发 C.蒸馏 D.升华
③必须冷却后才能取锌,是为了防止发生反应:(写化学方程式)。


①该小组分析溶解度曲线,推测析出的少量固体是NaCl,但检验后却发现是Na2SO4。请作出合理解释:。
②该小组停止蒸发浓缩,经、过滤得到大量Na2SO4固体及母液;将母液中的NaCl分离出来,操作是。
①甲同学向滴有酚酞溶液的氢氧化钙溶液中,逐滴滴加稀盐酸至足量,溶液由红色变成无色,证明溶液中,可判断Ca(OH)2与HCl发生了反应。
②乙同学将氢氧化钙溶液与稀盐酸混合,然后检验了混合液中含有Ca2+和Cl- , 他据此认为Ca(OH)2与HCl发生了反应,且生成了CaCl2。你认为乙同学是否找到了反应发生的证据?请说出你的观点并阐述理由:。

①分析A→B段变化,其他条件相同,导电能力:OH-Cl-。(填“>”“<”或“=”)
②分析B→C段变化,溶液的导电能力除了与离子种类有关,还与有关。
(本研究所用溶液很稀,密度均近似看作1g/cm3)
编号 | 浇灌液中CuSO4的 浓度 | 总体积/mL | 5%CuSO4溶液的 用量/mL | 水的用量/mL |
盆1 | 5% | 100 | 100 | 0 |
盆2 | 3% | 100 | 60 | 40 |
盆3 | 1% | 100 | a | b |
盆4 | w | 100 | c | d |
①补充盆3的配液数据:a=,b=。
②为了获得严谨的结论,合理设计盆4的配液方案:w=,d=。
①混合后产生大量白色沉淀,反应的化学方程式为。
②过滤,所得蓝色滤液中含有的溶质可能是:
假设一:只有CuCl2 假设二:CuCl2和BaCl2 假设三:。
③设计实验确定蓝色滤液的成分,完成下表:
|
实验操作 |
现象与结论 |
|
取少量滤液于试管中,。 |
说明假设二不成立。 |
|
。 |
,说明假设三成立。 |
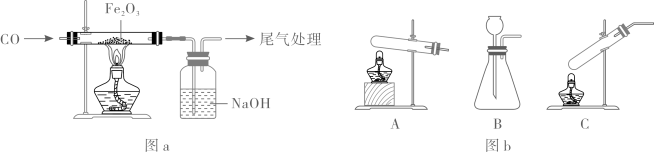
①定量分析物质组成可知,该反应生成Fe3O4是合理的,理由是。
②该小组通过对黑色固体进行检验,证明同时含有Fe3O4和Fe.检验的操作和现象是:取样于试管中,。

①用CO炼铁时,还原Fe2O3的温度应不低于℃。(填“400”“600”或“800”)
②图中:x=。
③该小组查阅资料得知酒精灯加热温度为600℃左右,他们发现上述对黑色固体成分的检验结果与图像有矛盾,推测黑色固体在冷却过程中发生了以下反应:。