
(猜想与假设)猜想一:CO、H2O;猜想二:;猜想三:CO2、CO、H2O。
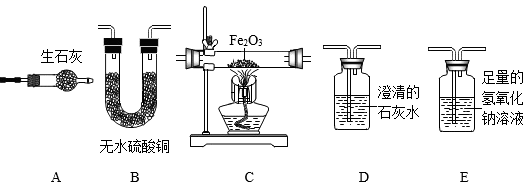
先将乙醇放入盛有一定量氧气的容器中燃烧,然后将燃烧产物通入上述装置,通入装置的顺序是(装置可以重复选用,也可以不选)。其中选用E装置的目的是。
(现象与结论)
实验中所选第一个装置观察到现象是,C中红棕色粉末变成黑色,D中澄清石灰水都变浑浊,由此推断猜想三成立。其中C装置内发生反应的化学方程式为。
实验结束后,小组同学对实验结论进行了反思:甲同学发现含碳的化合物燃烧时,氧气充足才能避免有毒物质一氧化碳产生;乙同学发现该实验的设计中有一个明显缺陷,该缺陷是。