
 高温煅烧一定质量的石灰石
B .
高温煅烧一定质量的石灰石
B .  用等质量、等浓度的双氧水分别制取氧气
C .
用等质量、等浓度的双氧水分别制取氧气
C .  向一定体积的水中逐滴加入氢氧化钠溶液
D .
向一定体积的水中逐滴加入氢氧化钠溶液
D .  某温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾晶体
某温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾晶体
小明同学取下列生活中的物质,测得其pH如表所示:
|
物质 |
石灰水 |
雨水 |
葡萄糖水 |
柠檬汁 |
食盐水 |
纯碱水 |
洁厕净 |
|
pH |
9.2 |
5.2 |
7.0 |
2.5 |
7.0 |
12.2 |
1.1 |
①酸性最强的物质是,能使无色酚酞试液变成红色的物质是。
②正常雨水显弱酸性。你认为其主要原因是(用化学方程式表示)。

上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为,由无水MgCl2制取Mg的化学方程式为。海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:。
1984年,地坛医院的前身北京第一传染病医院成功研制能迅速杀灭各类肝炎病毒的消毒液,定名为“84肝炎洗消液”,后更名为“84消毒液”。“84消毒液”是一种以次氯酸钠(NaClO)为主的高效消毒剂,呈无色或淡黄色液体,且具有刺激性气味,有效氯含量为5.5~6.5%。被广泛用于宾馆、旅游、医院、食品加工行业、家庭等场所的消毒。
空气中的CO2可以与NaClO反应得到次氯酸(HClO),反应的化学方程式为NaClO+CO₂+H₂O=NaHCO₃+HClO。HClO是一种比碳酸还弱的酸,但其具有极强的氧化性,能够将很多物质氧化,使其变性,因而能够起到消毒的作用。
NaClO不稳定,下图是对其稳定性的研究结果。

“84消毒液”在使用过程中要注意以下几点:
①需25℃以下避光保存,宜现用现配,一次性使用,勿用50℃以上热水稀释。
②有一定的刺激性与腐蚀性,必须稀释以后才能使用,使用时应戴手套,避免接触皮肤,对金属有腐蚀作用。
③漂白作用较强,对织物有漂白作用,慎用。如果浅色衣服染上其他颜色,也可以用其进行漂白。
④“84消毒液”是含氯消毒剂,消毒时容器必须加盖盖好,否则达不到消毒的效果。
⑤不要把“84消毒液”与其他洗涤剂或消毒液混合使用,因为这样会加大空气中氯气的浓度而引起氯气中毒。
准确了解和正确使用各类清洁剂可以为我们创造一种健康、安全、方便的生活。依据文章内容,回答下列问题:
A 对金属没有腐蚀作用
B 消毒时容器必须加盖盖好是因为易挥发出含氯物质
C 不要与其他洗涤剂或消毒剂混合使用是因为避免产生有毒的氯气
A小组同学发现实验台上摆放的药品中(如图),有一装溶液的试剂瓶未盖瓶盖且标签破损,于是决定对这瓶溶液进行实验探究:
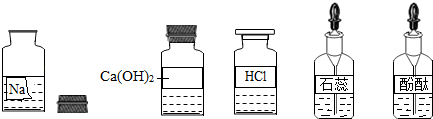
(提出问题)这瓶溶液是什么溶液?
(获得信息)
酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
(提出猜想)这瓶溶液可能是:1、氯化钠溶液;2、氢氧化钠溶液;3、碳酸钠溶液。
(实验推断)
(继续探究)另取样品加入过量的CaCl2溶液,可观察到有产生,反应的化学方程式为,设计这一步骤的目的是;静置后,取上层清液,滴入酚酞试液,溶液呈红色。
(探究启示)实验取完药品后应。
(提出问题)反应后溶液中溶质是什么呢?
(假设猜想)针对疑问,太家纷纷提出猜想。
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
|
实验方案 |
测溶液pH |
滴加Na2CO3溶液 |
滴加BaCl2溶液 |
|
实验操作 |
| | |
| 实验现象 | 试纸变色,对比比色卡,pH<7 |
| 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全组同学一致确定猜想二是正确的。
老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时指出实验探究(2)中存在两处明显不正确,请大家反思。同学们经过反思发现了这两处不正确:
①实验操作中的不正确是。
②实验方案中也有一个是错误的,错误的原因是。
你能再设计一个方案证明猪想二正确吗?方案是(包括实验过程、现象及结论,其中“实验过程”选择的药品不可以用酸碱指示剂,不可与上述实验方案中药品类别重复,“结论”的表述中能用化学方程式表示的要写出化学方程式)
|
步骤 |
现象 |
结论 |
|
|
|
|