一、<b >选择题(每题只有一个正确选项,每题</b><b >2.5</b><b>分)</b>
-
1.
下列变化中不涉及化学变化的是( )
A . 金刚石刀切割玻璃
B . 用粮食发酵酿酒
C . 生石灰吸水变成粉末
D . 铁矿石在高炉中炼铁
-
2.
空气中含量最多的气体是( )
A . 氧气
B . 二氧化碳
C . 氮气
D . 稀有气体
-
3.
下列物质中属于混合物的是( )
A . 蒸馏水
B . 苹果汁
C . 氧气
D . 干冰
-
4.
下列现象中,能充分说明“分子在不停的运动”的是( )
A . 春天,冰雪开始融化
B . 气体热胀冷缩
C . 真金不怕火烧
D . 墙内开花墙外香
-
-
6.
根据下列人体内一些液体的正常的pH范围判断,其中,一定能使石蕊溶液变红的是( )
A . 唾液(6.6~7.1)
B . 胆汁(7.1~7.3)
C . 胃液(0.9~1.5)
D . 血浆(7.35~7.45)
-
7.
硒是人体必需的微量元素.在元素周期表中硒元素的某些信息如图所示,下列有关硒的说法正确的是( )
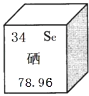
A . 属于金属元素
B . 原子序数为34
C . 原子核内中子数为34
D . 相对原子质量是78.96g
-
-
9.
如图是工业上将煤转化为清洁能源的微观示意图:

有关说法不正确的是( )
A . 图中  都属于氧化物
B . 该反应类型为置换反应
C . 反应前后原子的种类和数目保持不变
D . 一个
都属于氧化物
B . 该反应类型为置换反应
C . 反应前后原子的种类和数目保持不变
D . 一个 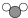 由一个氧原子和一个氢分子构成
由一个氧原子和一个氢分子构成
-
10.
合理施用化肥可提高农作物产量,但过多化肥如尿素[CO(NH2)2]等进入水体也会引起水体污染.尿素属于( )
A . 复合肥
B . 磷肥
C . 钾肥
D . 氮肥
-
11.
推理是一种重要的化学思维方法,以下推理合理的是( )
A . 因为MnO2能加快H2O2的分解速率,所以MnO2也能加快H2O的分解
B . 因为单质是由同种元素组成,所以只含一种元素的物质一定是单质
C . 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素
D . 中和反应一定有盐和水生成,所以有盐和水生成的反应一定是中和反应
-
12.
甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )

A . 甲的溶解度大于乙的溶解度
B . 20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数
C . 40℃时,分别在100 g水中加入40g 甲、乙,所得溶液溶质的质量分数相等
D . 分别将甲和乙的饱和溶液从40℃降低到20℃,甲会析出晶体,乙则不会
-
13.
甲、乙、丙和X,Y,Z都是初中化学中常见的物质,甲、乙、丙都是氧化物,且常温下甲固体,乙是气体,丙是液体.在一定条件下,甲、乙、丙之间存在如图所示的转化关系(反应条件和部分生成物已略去).下列判断正确的是( )

A . 甲一定是CuO
B . X一定具有还原性
C . Z一定是酸
D . Y和Z一定能发生反应
-
14.
下列各组物质的溶液,不用其它试剂,仅通过观察和用组内溶液相互混合的方法,不能将它们一一鉴别出来的是( )
A . NaOH、Ca(OH)2、HCl、K2CO3
B . NaCl、BaCl2、CuSO4、NaOH
C . Ba(OH)2、NaCl、Na2SO4、Na2CO3
D . AgNO3、HCl、Na2CO3、CaCl2
二、<b >填空题(本大题共包括</b><b >4</b><b>个小题,每空</b><b>1</b><b >分,共计</b><b >16</b><b>分)</b>
-
15.
化学,我们的生活,我们的未来!结合你所学的化学知识,回答下列有关的问题:
-
(1)
用化学符号表示:一个氢原子;两个二氧化碳分子.
-
(2)
根据“P2O5”回答:在五氧化二磷中,磷元素的化合价;磷元素与氧元素的质量比为.
-
16.
生活中处处有化学.请按要求回答下列问题:
-
(1)
自来水厂对天然水净化处理得到自来水的过程中,下列操作:①过滤;②吸附;③消毒;④蒸馏,没有用到的是.(填序号)
-
(2)
用自来水烧水的水壶底部,容易形成水垢,水垢的成分主要是碳酸钙和氢氧化镁,可以用厨房中的一种调味品来清除,这种调味品是.
-
(3)
为了防止人体缺碘,市售食盐中添加了少量的碘酸钾(KIO3),并在使用说明中强调“不宜高温烹煮”.碘酸钾与氯酸钾性质相似,试写出碘酸钾在加热条件下分解的化学方程式.
-
17.
节约能源、保护环境、低碳生活是全社会应该倡导的生活方式.
-
(1)
下列物质都可以用来作为燃料:①煤;②氢气;③石油;④天然气.其中,最清洁的燃料是(填序号).
-
(2)
充分燃烧1000g天然气和煤所产生的CO2和SO2气体的质量如图所示,根据图示分析,下列说法正确的是 . 
A . 煤燃烧产生的气体更易导致酸雨
B . 该天然气中不含硫元素
C . 煤燃烧对环境影响较小
D . 煤和天然气的燃烧都有温室气体产生
-
(3)
硫酸型酸雨的形成主要经过以下两步:①SO2在空气中被粉尘催化氧化得到SO3;②SO3与水化合形成硫酸.其中反应②的化学方程式为.
-
(4)
丙醇(化学式为C3H8O)是一种清洁燃料,它在一定量的氧气中燃烧的化学方程式可表示为C3H8O+4O2 4H2O+2CO2+X,生成物X的化学式为.要使6.0g丙醇燃烧时不生成X,则消耗氧气的质量至少为g.
4H2O+2CO2+X,生成物X的化学式为.要使6.0g丙醇燃烧时不生成X,则消耗氧气的质量至少为g.
-
18.
汽车是现代生活中重要的交通工具.请回答下列问题:
-
(1)
汽车电路中的导线一般为铜芯线,这是利用了金属铜的延展性和性.
-
(2)
下列制造汽车所用到的材料中,属于有机合成材料的是(填序号)
.
①钢铁 ②合成橡胶 ③羊毛织物 ④铝合金 ⑤塑料
-
(3)
铁在潮湿的空气中容易锈蚀.汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是隔绝和水.
-
(4)
某汽修厂清洗汽车零件后的废液中常含有一定量的AgNO
3和Cu(NO
3)
2 . 向AgNO
3和Cu(NO
3)
2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤液中加入稀盐酸,没有白色沉淀产生.下列叙述正确的是
(填序号).
A.滤渣中一定没有Fe B.滤液中一定有Fe(NO3)2和Cu(NO3)2
C.滤渣中一定有Ag,可能有Cu D.滤液中一定有Fe(NO3)2 , 一定没有AgNO3 .
三、<b >实验与探究(本大题共包括</b><b >2</b><b>个小题,每空</b><b>1</b><b >分,共计</b><b >11</b><b>分)</b>
-
19.
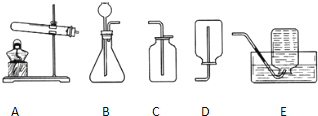
如图是实验室的部分实验装置,回答有关问题.
-
(1)
实验室用稀盐酸与石灰石反应制取二氧化碳应选用的装置是(填编号);其中,发生装置中产生CO2的化学方程式为.
-
(2)
检验二氧化碳是否集满的方法是;将适量的倒入集气瓶中震荡,观察到试剂变浑浊,说明该气体确实是二氧化碳.
-
20.
化学兴趣小组的同学将足量的锌粒加入到浓硫酸中,发现有大量的气泡放出,他们对气体的成分进行了探究.
【提出问题】锌粒加入浓硫酸后生成的气体是什么?
【查阅资料】
①浓硫酸能与锌反应,但不产生氢气,也不会产生氧气;
②SO2有刺激性气味,易溶于水,能使品红(一种红色色素)溶液褪色.
【提出猜想】
甲:气体是H2;
乙:气体是SO2;
丙:气体是SO2和H2;
【实验探究】
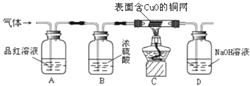
为了验证上述猜想.同学们在老师的指导下设计了如下图的装置(部分夹持器材略去,假设每个能发生的反应都完全进行)进行探究:
-
(1)
实验开始后,观察到A中品红溶液褪色,证明气体中含有.
-
-
(3)
C装置在点燃酒精灯加热之前应先通一段时间的气体,目的是;加热一段时间后,观察到,证明气体中含有H2 .
-
-
(5)
【讨论】
①锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气呢?用文字简述原因:.
②锌与浓硫酸和稀硫酸反应都可以产生硫酸锌,如果需要制取硫酸锌,用锌与稀硫酸反应的优点是(任填一种合理的答案).
四、<b >计算题(本大题包括</b><b >1</b><b>个小题,</b><b>8</b><b >分)</b>
-
21.
向盛有20.0g稀硫酸的烧杯中倒入5.0g黄铜(铜锌合金)样品粉末,恰好完全反应.称得未溶物质量为3.7g.完成下列计算:
①该黄铜样品中含Zn的质量为多少克?
②所用稀硫酸中溶质的质量分数
③反应后所得溶液中溶质质量分数(结果保留一位小数)

![]() 4H2O+2CO2+X,生成物X的化学式为.要使6.0g丙醇燃烧时不生成X,则消耗氧气的质量至少为g.
4H2O+2CO2+X,生成物X的化学式为.要使6.0g丙醇燃烧时不生成X,则消耗氧气的质量至少为g.