 用装置甲制取少量Cl2
B .
用装置甲制取少量Cl2
B .  用装置乙除去Cl2中的HCl
C .
用装置乙除去Cl2中的HCl
C .  用装置丙收集Cl2
D .
用装置丙收集Cl2
D .  用装置丁吸收尾气
用装置丁吸收尾气

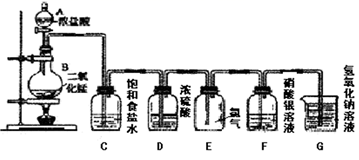
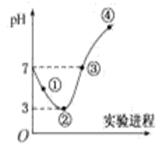

已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华。根据要求完成下列问题:



已知: 熔点-59℃、沸点11℃、
沸点150℃
中的化学方程式:
a.降低 的溶解度 b.减少
的分解 c.使
变为液态 d.加快反应速率



加热硬质玻璃管内铁丝约1 min,然后把注射器中的氯气注入到硬质玻璃管内,观察实验现象。硬质玻璃管内可观察到产生色的烟,盛硫氰化钾溶液的试管内显。
①KClO3与SO2在强酸性溶液中反应可制得ClO2 ,SO2被氧化为SO42- , 此反应的离子方程式为。
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl- , 该反应过程中氧化剂与还原剂的物质的量之比为。

在A装置中用固体二氧化锰与浓盐酸,在加热条件下制取氯气,写出反应的化学方程式;
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,可将装置如何改进。