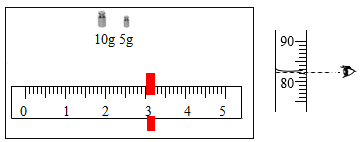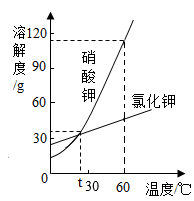
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 甲 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| 乙 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |
请回答下列问题:
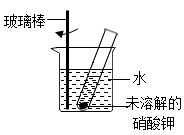
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体
A ①③④ B ②⑤⑥ C ①③⑤ D ②④⑥
A 水果、蔬菜 B 花生油、奶油 C 纯牛奶、蛋清 D 米饭、馒头
A 过氧乙酸(CH3COOOH) B 二氧化氯(ClO2)
C 苯酚(C6H6O) D 次氯酸钙[Ca(ClO)2]

请回答下列问题:
A 用少量水润湿滤纸,并使滤纸与漏斗壁之间留有气泡
B 漏斗下端的管口要紧靠烧杯内壁
C 玻璃棒要靠在三层滤纸的一边
D 滤纸边缘要低于漏斗口,液面要低于滤纸边缘