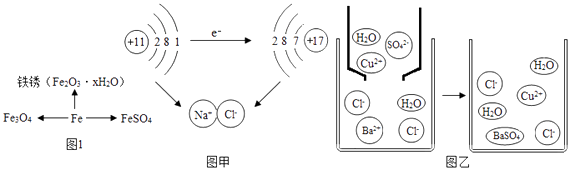
①铁丝燃烧生成Fe3O4的过程中(选填“放出”或“吸收”)热量.
②铁制品的锈蚀过程,实际上是铁与空气中的等发生化学反应的过程.
③与FeSO4中铁元素化合价相同的铁氧化物的化学式是.
①图甲是钠与氯气反应生成氯化钠的示意图.该图说明在化学反应过程中一定发生变化的是.(填字母)
a.原子核 b.原子核最外层电子数 c.原子的电子层数
②图乙是硫酸铜溶液与氯化钡溶液反应示意图.从粒子角度分析该化学反应能发生的原因是.

①实验1中同时向烧杯中加入一粒相同大小的品红,发现整杯水变红的时间热水比冷水短.这是因为.
②实验2中使用铜片是为了对比不同.
③实验3是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体.下列结论不正确的是(填字母).
a.铜不能发生置换反应
b.四种金属中金属活动性最强的是Mg
c.等质量的锌和铁分别与足量的盐酸发生生成气体质量:Zn比Fe多.
①过滤操作中玻璃棒的末端要轻轻的斜靠在一边.蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是.
②下列操作可能导致精盐产率偏高的是(填字母)
a.食盐没有完全溶解即过滤 b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到称量纸上
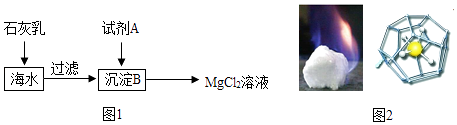
①在海水中加入石灰乳后,发生反应的化学方程式是.
②上述过程中试剂A与沉淀B法神的是中和反应,则试剂A是(填名称).
①可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于(选填“纯净物”或“混合物”).
②若某种可燃冰中CH4与H2O的质量比是1:9,则该可燃冰中n=.
③可燃冰中甲烷完全燃烧的化学方程式是.
【查阅资料】
Ⅰ.过碳酸钠在水中易离解成Na2CO3和H2O2 , 其水溶液具有Na2CO3和H2O2的双重性质;
Ⅱ.过碳酸钠与盐酸反应:2(2Na2CO3•3H2O2)+8HCl═8NaCl+4CO2↑+3O2↑+10H2O;
Ⅲ.过碳酸钠的去污能力主要与其在反应中释放处的“活性氧”有关,“活性氧”含量越高,去污能力越强.
“活性氧”含量= ×100%
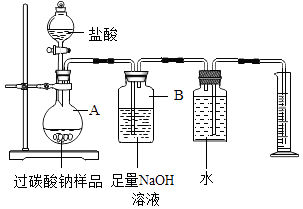
为测定某过碳酸钠样品中“活性氧”含量,取20g样品按如图实验装置与足量盐酸反应.(已知样品中杂质不溶于水且不与盐酸反应,装置气密性良好)
①将盐酸慢慢地入A中,反应一段时间,观察到,停止滴加盐酸.
②装置B可吸收生成的CO2 , 该反应的化学方程式是.
③甲同学认为若要得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下的.
④将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量,写出其计算过程 .
⑤完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO2的质量,据此可计算出样品中“活性氧”含量.但丁同学认为该方案不合理,丁同学的理由是(填写一条即可)