| 选项 | 物质 | 杂质 | 操作 |
| A | CaO | CaCO3 | 加入过量的水,过滤 |
| B | 盐酸 | 硫酸 | 加入过量的BaCl2溶液,过滤 |
| C | NaNO3溶液 | NaCl溶液 | 加入过量的AgNO3溶液,过滤 |
| D | CaCl2溶液 | 稀盐酸 | 加入过量的CaCO3粉末,过滤 |
Ⅰ.取少量固体样品于烧杯中,先加足量水溶解,再加入足量的BaCl2溶液,有白色沉淀产生;
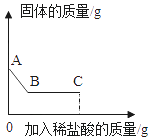
Ⅱ.继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示.
请回答下列问题:

【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液;猜想三:碳酸钠溶液。
【实验推断】
⑴小丽取样滴加无酚酞试液,溶液呈红色。
⑵小刚另取样滴加稀盐酸有产生,小刚得出结论:该溶液是碳酸钠溶液。
⑶小青认为小刚的结论不完全正确,理由是。
小组同学讨论后一致认为还需要进行如下实验:
【继续探究】另取样加入过量的CaCl2溶液,观察到有白色沉淀产生,设计这一步骤的目的是;静置后,取上层清液,滴入酚酞试液,溶液呈红色。
【实验结论】猜想是正确的。
【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应。

【实验步骤】①按如图连接好装置后,发现一处明显的错误,改正为;
②重新连接好装置,并再次检查装置的气密性;
③在B装置中加入牙膏样品8g
④关闭K1 , 打开K2 , 向牙膏样品中滴入10%的盐酸,至B中无气泡产生时,停止滴加盐酸;
⑤关闭K2 , 打开K1缓缓地通入空气,至C中不再产生沉淀;
⑥将C装置中的固液混合物过滤、洗涤、烘干后称量其质量。
![]()
【实验分析及数据处理】
①若没有A装置,则测定结果将(填“偏大”、“偏小”或“不变”)。
②D装置的作用是
③据上面数据,计算该牙膏样品中碳酸钙的质量分数是