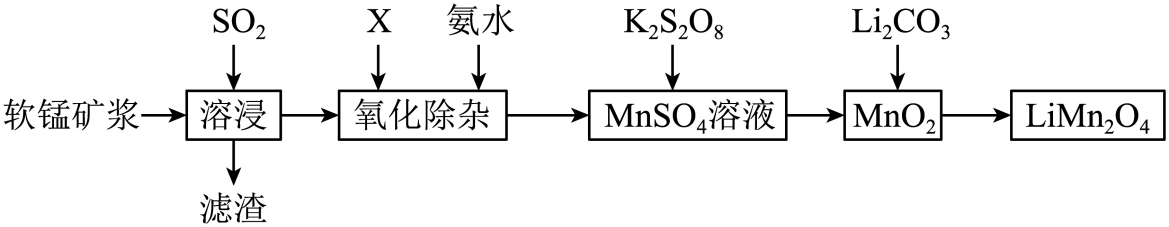
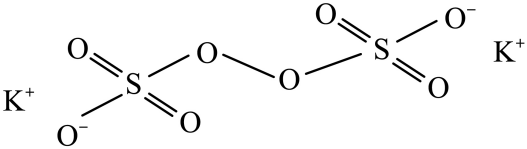
 )溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。
)溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。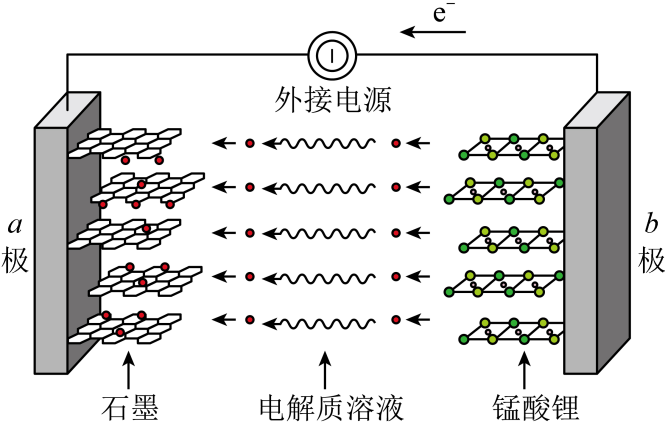
①放电时,电池正极的电极反应式为。
②充电时,向极移动(填“a”或“b”)。
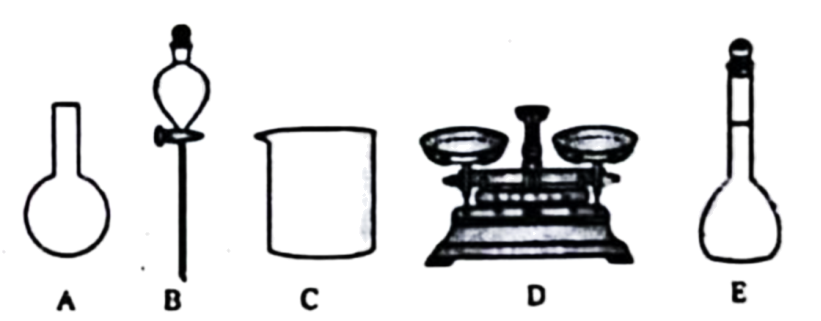
①写出在配制过程中,上图所示的仪器,用不到的仪器名称。
②配制过程中,需称量该漂白粉的质量为g
③该同学配制溶液后,发现溶液底部中有少量不溶物。请用化学方程式写出形成其不溶物的原因。
①需用浓硫酸的体积为。
②取用任意体积的浓硫酸时,下列物理量中不随所取体积的多少而变化的是。
A.溶液中的物质的量 B.溶液的浓度
C.溶液的质量 D.溶液的密度
③在浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于2.3有。
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.定容时俯视观察液面
D.量取浓硫酸时俯视凹液面