①已知下列数据:
化学键 | H-H | C-H | H-O | C=O |
断裂化学键吸收的能量/(kJ·mol-1) | 435 | 415 | 465 | 800 |
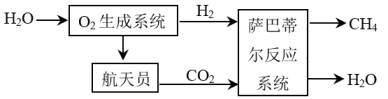
则“萨巴蒂尔反应”的热化学方程式为。
②“萨巴蒂尔反应”在固定容积的密闭容器中发生,若要提高CO2的平衡转化率,可采取的措施有(写两条)。
①CO2的富集与转化是O2再生的核心问题。“电化学富集法”是一种适合飞行器较长时间飞行的方法,装置如图所示。b极为极(填“正”或“负”),a电极上发生的电极反应为。
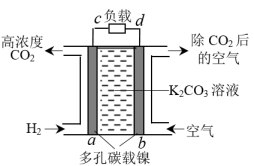
②负载中电解水可实现O2的再生,阳极为(填“c”或“d”),电极反应为。
③下列措施可提高O2生成速率的是。
A.提高电解时的电源电压 B.向水中加入少量的NaCl
C.适当提高电解液的温度 D.用金属铜作阳极
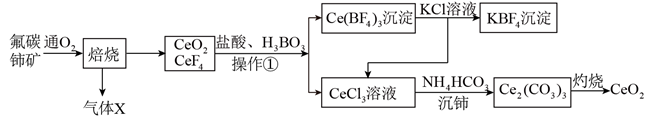
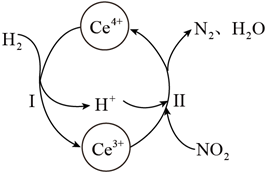
①该反应中的催化剂为(写离子符号)
②该转化过程中氧化剂与还原剂物质的量之比为。
物质 | |||
0.0 |
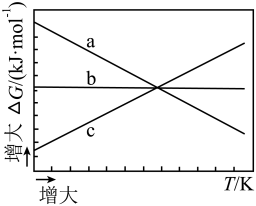

①根据元素电负性的变化规律,图中反应步骤Ⅲ可描述为。
②在合成甲醇过程中,需要不断分离出甲醇的原因为(填选项字母)。
a.有利于平衡正向移动b.防止催化剂中毒c.提高正反应速率
①内,
。
②反应ⅲ的平衡常数(保留三位有效数字)。
①需控制出气流量小于进气流量的原因为。
②已知出气流量为 , 单位时间内
的转化率为60%,则流出气体中
的百分含量为。