断开(或形成)1mol化学键的能量变化数据如下表所示,利用下表中的数据可知,该反应每生成1mol甲醇,需要(填“吸收”或“放出”)kJ的热量。
化学键 | H-H | C-O | C=O | O-H | C-H |
436 | 326 | 803 | 464 | 414 |
①
②
③
计算热分解反应④
。
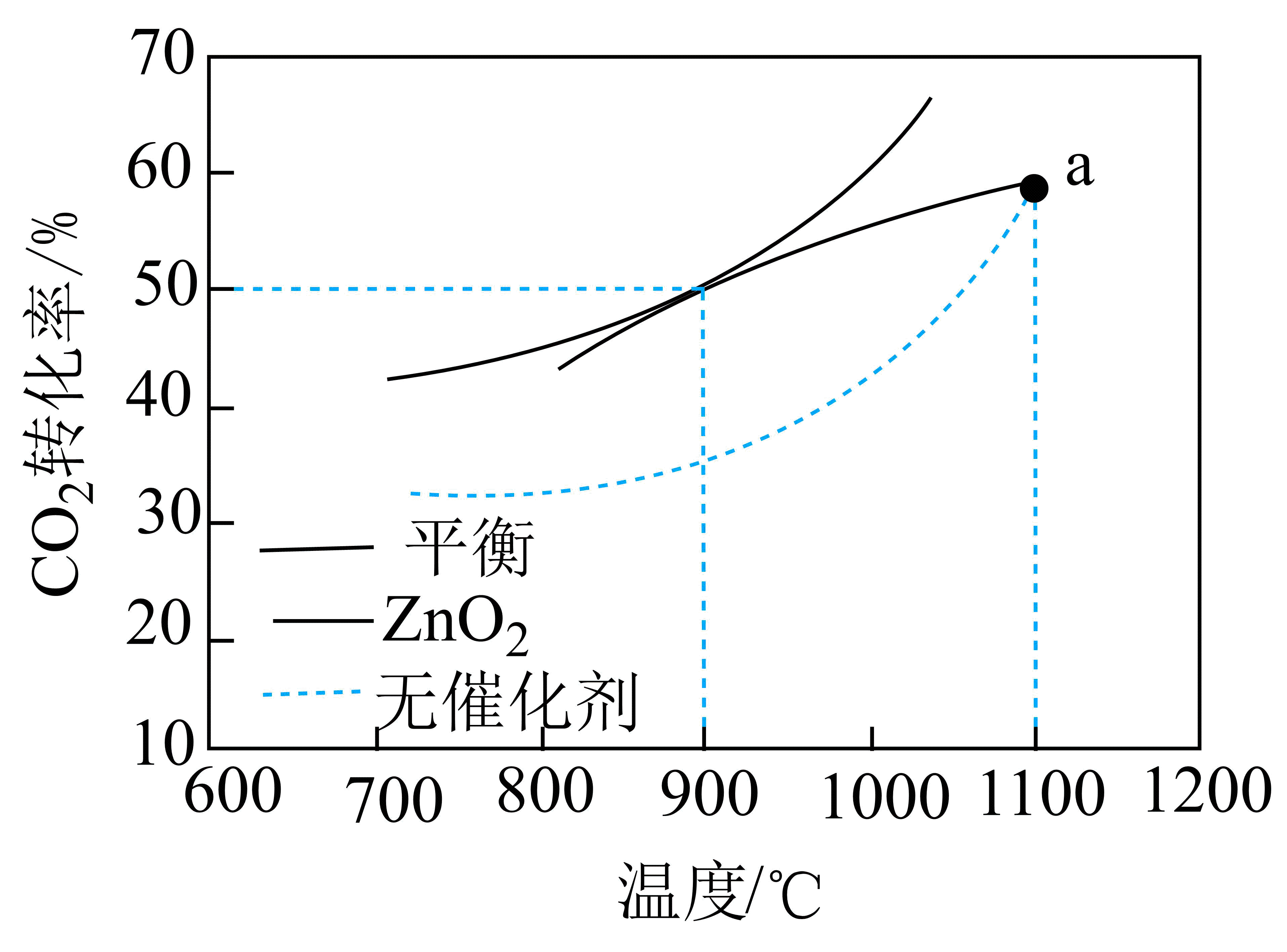
在pMPa、900℃、催化条件下,将
、
、
按物质的量之比为
充入密闭容器,
的平衡转化率为
, 此时平衡常数
(以分压表示,分压=总压×物质的量分数;写出含
、
、
的计算表达式)。
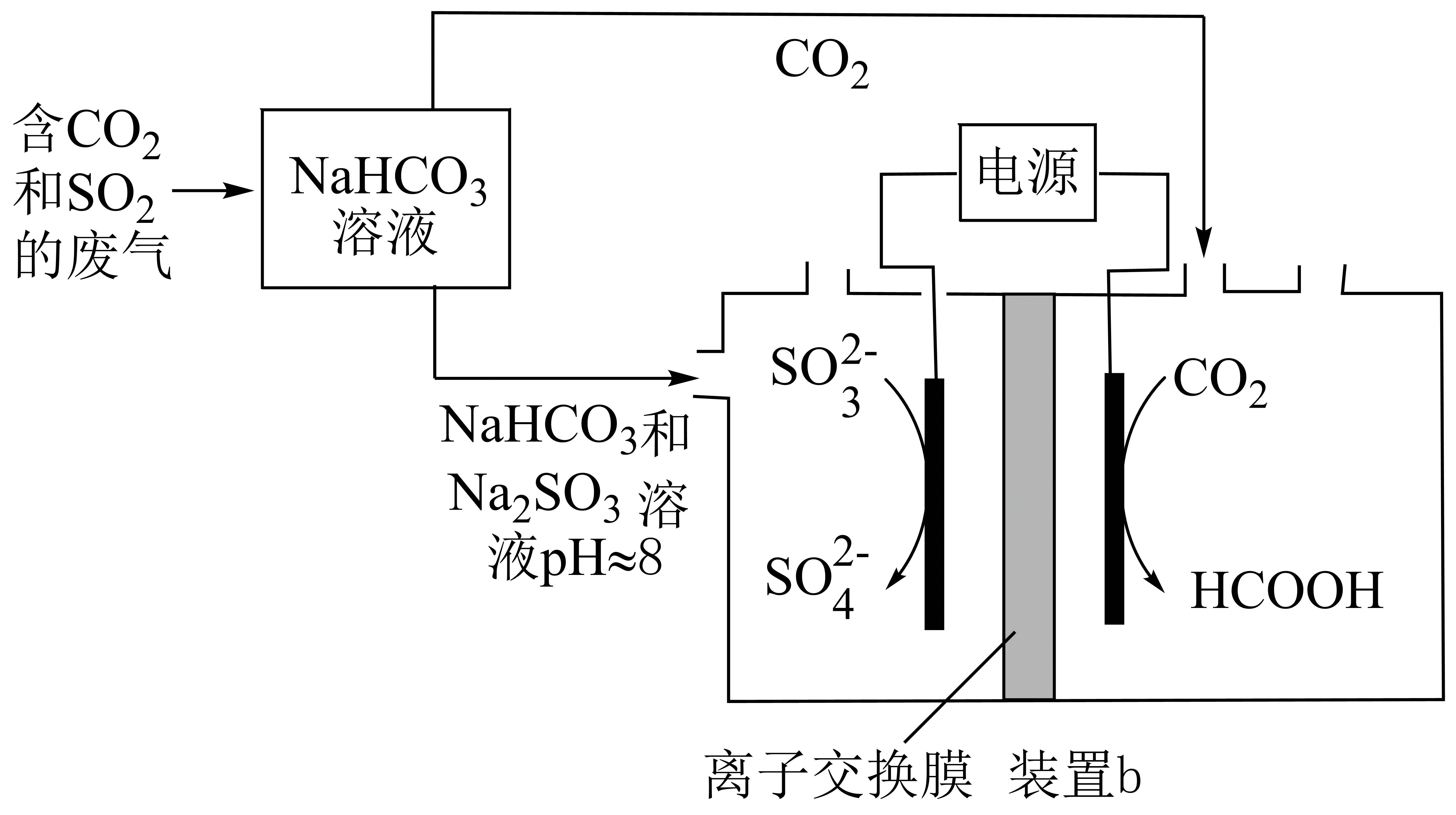
①装置b中参与反应的电极为极(填“正”、“负”、“阴”或“阳”)
②反应后装置b中溶液pH变化(填“增大”、“减小”或“不变”)
③装置b中的总反应的离子方程式为。