1.
(2023高三上·浙江月考)
亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,熔点:-64.5℃,沸点:-5.5℃,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可用下图装置由氯气与一氧化氮在常温常压下合成。
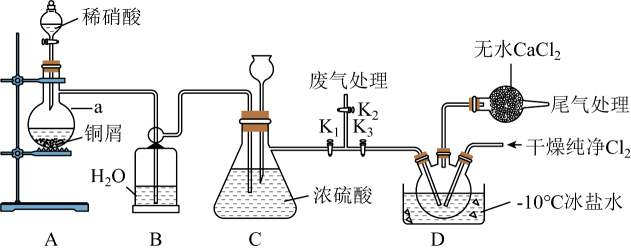
简要步骤如下:实验开始时,关闭 , 打开
, 打开 、
、 , 通入一段时间的氯气,直至三颈烧瓶中充满黄绿色气体,关闭
, 通入一段时间的氯气,直至三颈烧瓶中充满黄绿色气体,关闭 , 打开
, 打开 , 打开分液漏斗塞子,向装置a中滴入适量稀硝酸。待装置C中某一现象发生时,关闭
, 打开分液漏斗塞子,向装置a中滴入适量稀硝酸。待装置C中某一现象发生时,关闭 , 打开
, 打开 , 在三颈烧瓶中制备亚硝酰氯。
, 在三颈烧瓶中制备亚硝酰氯。
请回答:
-
-
-
(2)
写出亚硝酰氯与NaOH溶液反应生成亚硝酸钠的化学方程式:。
-
-
-
-
-
-
(5)
下列说法不正确的是____。
A . 从安全或避免环境污染方面考虑,宜在通风橱内进行实验
B . 若不慎亚硝酰氯接触到皮肤,及时用流动清水反复冲洗
C . 浓硫酸和无水 仅起阻止水蒸气进入,避免亚硝酰氯水解的作用
D . 冰盐水温度可达-10℃,装置D三颈烧瓶中充满黄色气体NOCl
仅起阻止水蒸气进入,避免亚硝酰氯水解的作用
D . 冰盐水温度可达-10℃,装置D三颈烧瓶中充满黄色气体NOCl
-
-
(6)
若制得的NOCl中含有少量

杂质,为测定产品纯度进行如下实验:称取1.6625g样品溶于50.00mLNaOH溶液中,加入几滴

溶液作指示剂,用足量硝酸酸化的

溶液滴定至产生砖红色沉淀,消耗

溶液50.00mL。则样品的纯度为
%(保留1位小数)。
-

, 打开
、
, 通入一段时间的氯气,直至三颈烧瓶中充满黄绿色气体,关闭
, 打开
, 打开分液漏斗塞子,向装置a中滴入适量稀硝酸。待装置C中某一现象发生时,关闭
, 打开
, 在三颈烧瓶中制备亚硝酰氯。