①COCl2中C、O和Cl元素的电负性由大到小的顺序是 (用元素符号表示)。
②CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2分子的空间构型是 (填“平面四边形”或“四面体形”)。

①阴离子中碳原子的杂化轨道类型是。
②在丙二酸根与Cr3+配位时,配位原子为1号氧而不是2号氧的原因是。
①下列为晶胞中Cr原子沿x轴方向的投影的是( 填字母)。
a.  b.
b. 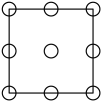 c.
c. 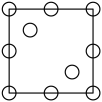 d.
d. 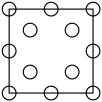
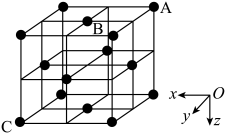
②若晶胞中最近的Cr原子和N原子相切,原子半径分别为r(Cr) nm和r(N) nm;晶胞中N原子的坐标是A(0,0,0)、B( ,
, 0) ,则距A和B最近的Cr原子的坐标是,该原子到C原子的距离是nm[用含r(Cr)、r(N)的代数式表示]。