1.
(2022·四平模拟)
金属磷化物(如磷化锌)是常用的蒸杀虫剂。我国卫生部门规定:粮食中磷化物(以PH3计)的含量不超过0.050mg:kg-1时,粮食质量方达标。现设计测定粮食中残留磷化物含量的实验如下
【资料查阅】磷化锌易水解产生PH3;PH3沸点为-88℃,有剧毒性、强还原性、易自然。
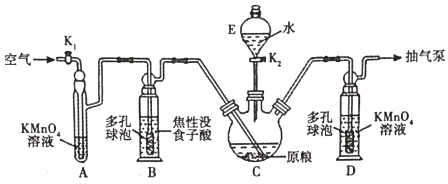
【用量标准]如图:装置A、B、E中盛有的试剂均足量;C中装有100原粮;D中盛有40.00mL6.0×10-5mol・L-1KMnO4溶液(H2SO4酸化)。
【操作流程】安装仪器并检查气密性→PH3的产生与吸收一转移KMnO4吸收溶液→用Na2SO3标准溶液滴定。
试回答下列问题:
-
(1)
仪器E的名称是;仪器B、D中进气管下端设计成多孔球泡形状,目的是。
-
-
(2)
A装置的作用是;B装置的作用是吸收空气中的O2 , 防止。
-
-
(3)
下列操作中,不利于精确测定出实验结果的是
(选填序号)。
a.实验前,将C中原粮预先磨碎成粉末
b.将蒸馏水预先煮沸、迅速冷却并注入E中
c.实验过程中,用抽气泵尽可能加快抽气速率
-
-
(4)
磷化锌发生水解反应时除产生PH3外,还生成(填化学式)。
-
-
(5)
D中PH3被氧化成H3PO4 , 该反应的离子方程式为。
-
-
(6)
把D中吸收液转移至容量瓶中,加水稀释至250.00mL,取25.00mL于锥形瓶中,用 5.0×10-5mol・L-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液10.00mL.则该原粮中磷化物(以PH3计)的含量为mg・kg-1 , 该原粮质量(填“达标”或“不达标“)。
-
