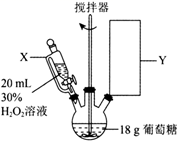
仪器X的名称为,Y处为冷凝回流装置,下列仪器使用正确且效果最好的是(填字母)。

用移液管取出三口烧瓶中的反应液2.00mL置于锥形瓶中,以酚酞作为指示剂并加20mL蒸馏水稀释,用0.04mol·L-1NaOH标准溶液滴定。
①滴定管使用的正确的操作顺序为蒸馏水洗涤→标准液润洗→→→→→洗净→放回滴定管架(填字母)。
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②达到滴定终点时的现象为。
③滴定过程消耗NaOH标准溶液的体积为V0mL,反应后三口烧瓶内溶液的体积为V1mL,实验条件下葡萄糖的转化率为(用含V0和V1的代数式表示)。
④若滴定终点时俯视读数,对转化率的影响为(填“偏高”“偏低”或“无影响”)。
将CaCO3分散于适量蒸馏水中形成浊液,加入葡萄糖酸,至无CO2气体放出为止,煮沸,并趁热采用下图装置抽滤,滤掉未反应的CaCO3 , 得到澄清透明的葡萄糖酸钙溶液。

抽滤时自来水流的作用是使瓶内与大气形成压强差,与普通过滤操作相比,抽滤的优点是。