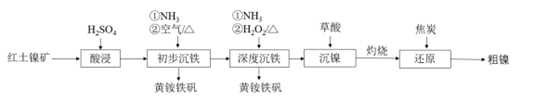
①溶液中Fe3+转化为黄铵铁矾的离子方程式为。
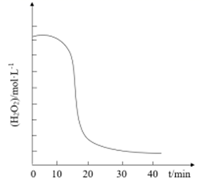
②溶液中c(H2O2)随时间t的变化关系如图所示,反应开始10~20 min内c(H2O2)迅速减小,其原因是。
|
金属离子的氢氧化物 |
Ni(OH)2 |
Fe(OH)3 |
黄铵铁矾 |
|
开始沉淀pH |
7.1 |
2.7 |
1.3 |
|
沉淀完全pH |
9.2 |
3.7 |
2.3 |
“深度沉铁”中通入NH3调节溶液pH的范围是。