
已知:部分金属氢氧化物的pKsp(pKsp=-lgKsp)的柱状图如图1。
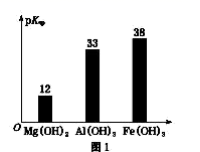
回答下列问题:
①锂辉石的主要成分为LiAlSi2O6 , 其氧化物的形式为。
②为提高“酸化焙烧”效率,常采取的措施是。
③向“浸出液”中加入CaCO3 , 其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、Al3+完全沉淀,则pH至少为。(已知:完全沉淀后离子浓度低于1×10-5)mol/L)
④“沉锂”过程所获得的“母液”中仍含有大量的Li+ , 可将其加入到“”步骤中。
⑤Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为
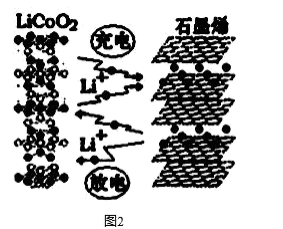
下列关于该电池的说法正确的是___________(填字母)。