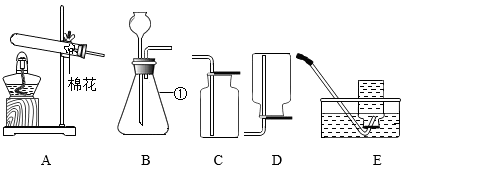
为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热.
Ⅱ.将X g KClO3与1.0g CuO均匀混合加热.
在相同温度下,比较两组实验产生O2的快慢.
Ⅱ中X的值为.
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
本实验中,测量O2的装置是(填序号).
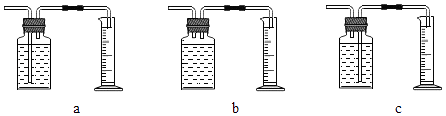
实验结论:在相同条件下,,双氧水分解的快,丙用如图2装置进行实验,通过比较也能达到实验目的.
湿法炼铜记载于西汉时期《淮南万毕术》:曾青得铁则化为铜。说明铁的金属活动性比铜(填“强”或“弱”)。
有文献报道:在氢气还原氧化铜的一些实验中,得到的固体产物是铜和氧化亚铜(Cu2O)组成的混合物。氧化亚铜为红色固体,在空气中溶于氨水得到蓝色溶液。某兴趣小组对此开展如下探究。
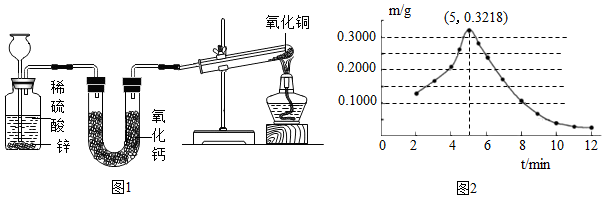
设计如图1所示的实验装置,开展氢气还原氧化铜实验并检验固体产物。
①实验开始时,(填序号)。
A.先点燃酒精灯加热后向长颈漏斗中加稀硫酸
B.先向长颈漏斗中加稀硫酸后点酒精灯
②取反应后的红色固体于烧杯中,加入氨水并搅拌,观察到,证明固体产物Cu2O。
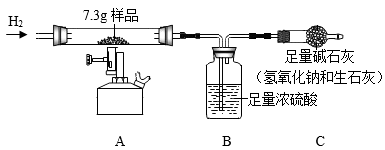
称取若干份质量均为0.6000g的CuO,在相同条件下分别用氢气还原不同时间(t),检测所得固体中Cu2O的质量(m),结果如图2。
①为确保氢气还原氧化铜所得固体产物不含Cu2O,应采取的措施是。
②在冶金工业中,氢气还原金属氧化物和传统碳还原相比,主要优点在于。
实验前先通一会儿氢气的原因是。
该生铁粉中铁元素的质量是g。