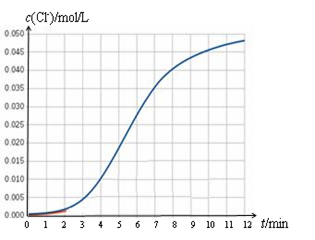
已知:ClO3− + 3HSO3−=Cl− + 3SO42− + 3H+
|
方案 |
假设 |
实验操作 |
|
I |
该反应放热,使溶液温度升高,反应速率加快 |
向烧杯中加入10mL0.1mol/LKClO3溶液和10mL0.3mol/LNaHSO3溶液,………… |
|
II |
………… |
取10mL0.1mol/LKClO3溶液加入烧杯中,向其中加入少量NaCl固体,再加入10mL0.3mol/LNaHSO3溶液。 |
|
III |
溶液酸性增强加快了化学反应速率 |
分别向2只烧杯中加入10mL0.1mol/LKClO3溶液;向烧杯①中加入1 mL水,向烧杯②中加入1mL0.2mol/L 盐酸;再分别向2只烧杯中加入10mL0.3mol/LNaHSO3溶液。 |
①补全方案I中的实验操作:。
②方案II中的假设为。
③除I、II、III中的假设外,还可以提出的假设是。
④在已知方案 I 的假设不成立的情况下,某同学从控制变量的角度思考,认为方案III中实验操作设计不严谨,请进行改进:。
⑤反应后期,化学反应速率变慢的原因是。