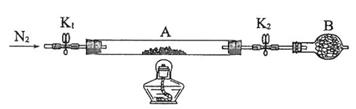
①仪器B的名称是。
②将下列实验操作步骤正确排序(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2 , 缓缓通入N2 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=(列式表示)。若实验时按a、d次序操作,则使x(填“偏大”“偏小”或“无影响”)。

①C、D中的溶液依次为(填标号)。C、D中有气泡冒出,并可观察到的现象分别为。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式。
方法一:在高温下,通入水蒸气将煤样中无机盐转化为HCl,再滴定氯离子。
方法二:取a g煤样,处理后得到含氯离子的样品溶液,加入溶液,以
作指示剂,用
溶液滴定过量的
溶液,共消耗KSCN溶液
。
已知:能与KSCN反应生成AgSCN沉淀。
①结合化学用语,从化学平衡的角度解释方法一中无机盐中生成HCl的原因。
②方法二中,滴定终点的现象为。
③利用方法二,测得煤样中氯元素的质量分数为。
i.配制固定组分的铬酸银()浑浊液;
ii.将待测海砂样品与i中浑浊液混合,溶液的颜色会随着氯离子含量的变化而变化。
氯离子含量x | |||
ii中现象 | 沉淀仍然为砖红色 | 砖红色沉淀部分变为白色,溶液逐渐转变为黄色 | 砖红色沉淀完全变为白色,溶液完全转变为黄色 |
已知:;
;
溶液为黄色,
固体为砖红色。
①时,沉淀仍然为砖红色的原因是。
②写出砖红色沉淀变为白色的离子方程式。

