
①仪器f和j的名称分别为、。
②在分液操作中,必须用到的仪器是(填字母,下同)。
③能作反应容器且可直接加热的仪器是。
④过滤时,需要用到的玻璃仪器是
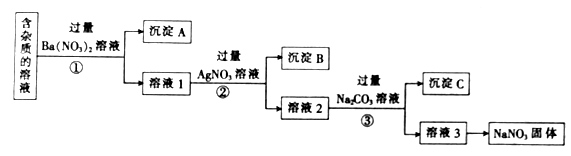
①配制溶液前要先计算,需称取NaNO3固体g。
②某同学转移溶液的操作如图所示,图中仪器的名称是烧杯和,该同学操作中的错误是。
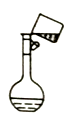
③若用胶头滴管定容时,不小心加水超过了刻度线,则应该采取的处理方法是。
④下列操作中,可能造成所配制溶液的浓度偏低的是(填字母)。
a.没有洗涤烧杯和玻璃棒
b.定容时,俯视刻度线
c.洗涤后的容量瓶中残留少量蒸馏水