A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
B元素原子的核外p电子数比s电子数少1 |
C元素基态原子p轨道有两个未成对电子 |
D原子的第一至第四电离能分别是: |
E原子核外所有p轨道全满或半满 |
F在周期表的第8纵列 |
 , 该同学所画的电子排布图违背了。
, 该同学所画的电子排布图违背了。
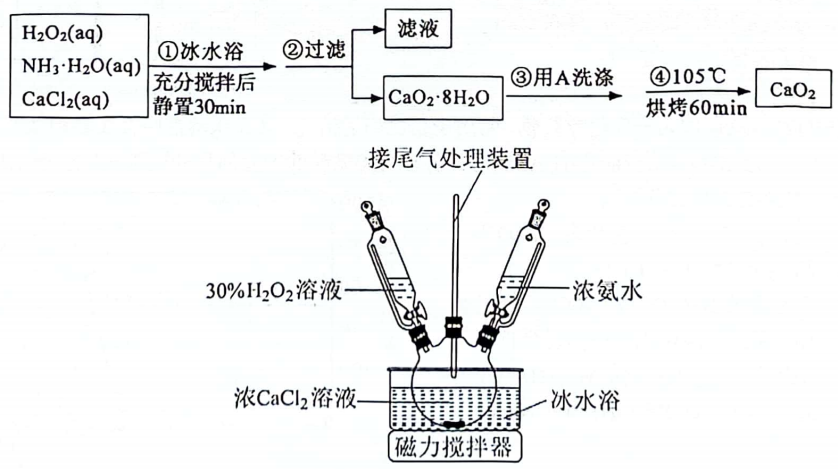
a.水 b.乙醇 c.盐酸
第一步:准确称取产品于烧杯中,加入适量的盐酸使其完全溶解;
第二步:向上述溶液中加入稍过量的 , 形成
沉淀,过滤并洗涤沉淀;
第三步:将洗涤好的沉淀用稍过量的稀硫酸溶解,溶解液和洗涤液全部转移至锥形瓶中;
第四步:因反应较慢,向锥形瓶中滴入几滴溶液,然后逐滴滴入浓度为
的
溶液至终点,消耗
溶液
。
①滴定前,滴入溶液的目的是。
②滴定终点的现象为。
③产品的纯度为(用字母表示)。
④若第三步用稀盐酸溶解,所测纯度(填“偏低”“不变”或“偏高”)。

金属离子 | |||
开始沉淀时的 | 6.3 | 2.2 | 8.9 |
完全沉淀时的 | 9.0 | 2.8 | 10.9 |
上述流程中所用“氧化剂”常用双氧水,这一步不可省掉的理由是。
物质 | |||
相对能量/( | -393 | 0 | -423.9 |
则=
。反应中应控制合适的投料比,随
与
的投料比增大,
的转化率将。
A | B | C | D |
|
|
|
|
。维持容器容积1L不变,按照固定投料比将
和
按一定流速通过该催化剂,平衡时,测得如下数据:
温度(K) |
| 甲酸选择性(%) |
323 | 40.0 | 50.0 |
343 | 54.6 | 48.3 |
注:甲酸的选择性是指发生反应的中转化为甲酸的百分比。
①数据表明,升高温度,转化率提高而甲酸选择性降低,其原因是;
②323K下,与
各按1mol投料,平衡时,
的物质的量为,主反应的平衡常数
=。