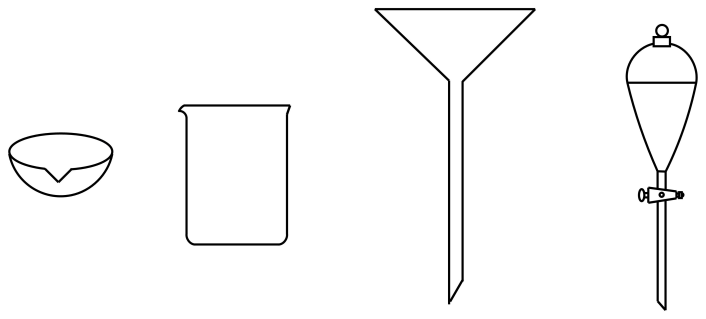
a.酸 b.碱 c.盐 d.氧化物
①配制时应选用容量瓶,用电子天平称取
固体的质量是
。
②配制过程中,下列操作会引起所配溶液浓度偏高的是(填序号)。
a.容量瓶用蒸馏水洗净后未烘干 b.定容时俯视
c.加蒸馏水时不慎超过了刻度 d.未冷却至室温就开始定容
①与
反应的化学方程式是。某潜水艇一天约需
(标准状况),假设所需
全部由上述反应来提供,则该潜水艇一天所需要的
的质量是
。
②将一定量的投入到含有
、
、
、
的溶液中,反应完毕后,溶液中上述离子数目几乎不变的是(填离子符号)。

a.、
的单质与铁反应分别生成
、
b.能从
中置换出
单质
c.相同温度下,的溶解度比
的大
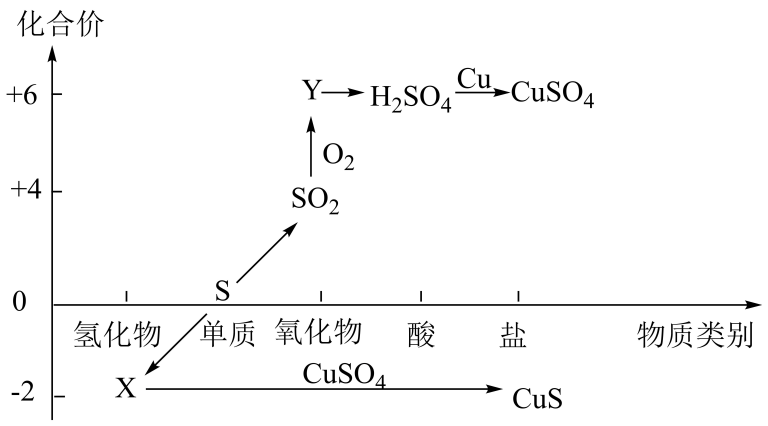
①请用“双线桥”法标明该反应电子转移的方向和数目。
②当有电子发生转移时,理论上生成
的体积(标准状况)为
。
已知黄铁矿与氧气反应的化学方程式是
Ⅰ.实验室将固体与浓硫酸混合加热制取
。
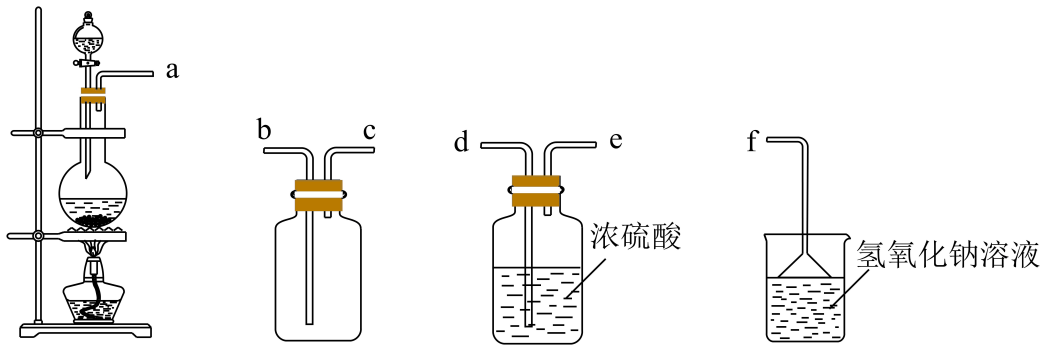

已知:①制备三氯硅烷的化学方程式:
②三氯硅烷的熔点 , 沸点
;极易与水反应,易被氧化。
装置所装药品是(填“碱石灰”或“无水氯化钙”),加热前要先通一段时间
气体,原因是。
a.过滤 b.萃取 c.蒸发结晶 d.蒸馏
Ⅰ.的一种制备方法如下图所示:

Ⅰ.的一种制备方法如下图所示:


已知:①;
②碘微溶于水,从左右开始升华;
的沸点是
。
海带浸取原液在酸性条件下被氧化的离子方程式是。