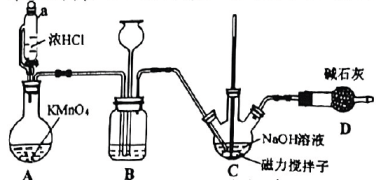
已知: , 若温度超过
, 会生成
杂质.
回答下列问题:

84消毒液和医用酒精均为重要的消毒剂且二者不能混用,某小组对84消毒液与医用酒精的反应产物进行了探究.
【提出假设】医用酒精中的被氧化为
【实验方案】实验方案及现象如下:
实验操作 | 取样检测时间点 | 实验现象 |
常温下将 | ① | |
橙黄色沉淀 | ||
黑色沉淀 |
【实验结论1】产物中有乙醛,且乙醛会被转化为其它物质.补充①的实验现象:.
【查阅资料】混合体系中可能发生以下反应:
(卤化反应)
【实验设计】取2份84消毒液,缓慢滴加医用酒精或蒸馏水各
, 通过测定过程中
变化判断是否发生卤化反应(忽略过程中的热效应对
的影响).实验结果如图.

【实验结论2】数据表明,反应过程中增大,说明乙醛发生了卤化反应.
【查阅资料】某同学查阅资料后认为结论2不严谨,原因是工业上为了稳定 , 在84消毒液中添加了少量
, 且由于乙醇的“锁水”效应也会使
增大(提示:乙醇与
不反应).
【数据分析】②已知上述实验:84消毒液中 .
通过计算证明84消毒液中添加了少量 , 写出计算过程.
【实验总结】医用酒精中的乙醇能被84消毒液氧化为乙醛,乙醛能进一步发生卤化反应.

已知:常温下;
为第四周期第ⅤA族元素;高铼酸铵微溶于冷水,易溶于热水.
回答下列问题:

图1:高铼酸铵谱 图2
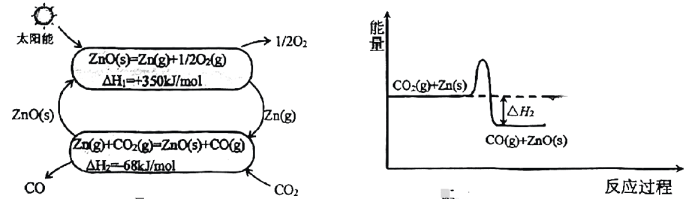
图3 图4
①晶体的
模型为.
②的反应过程如图3,在图4中仿照第一步反应画出第二步反应过程的能量变化示意图.
③科研小组尝试利用固体表面催化工艺进行
的分解.若用●、○和
![]() 分别表示C原子、O原子和固体催化剂,在固体催化剂表面分解
分别表示C原子、O原子和固体催化剂,在固体催化剂表面分解的过程如下图所示.下列有关说法中正确的是.
![]()
A.固体催化剂降低了反应的 B.过程③体系能量降低
C.过程②有键的断裂 D.整个过程中形成了头碰头的
键
主反应Ⅰ:
副反应Ⅱ:
④一定条件下,的平衡转化率及平衡时
的选择性(生成
所消耗的
与
消耗总量的比值)随温度变化如图所示.下列说法不正确的是.

A.增大压强,反应Ⅰ平衡正向移动,反应Ⅱ平衡不移动
B.当容器中不变时,两个反应均达到最大限度
C.
D.选用合适的催化剂可提高二甲醚的选择性
⑤图中后
平衡转化率升高的原因为.
⑥在下,将
和
通入
刚性容器中发生反应Ⅰ、Ⅱ,
时达到平衡,测得
的转化率为60%,容器中
的浓度为
, 则
(用含t的式子表示),反应Ⅰ的平衡常数
.
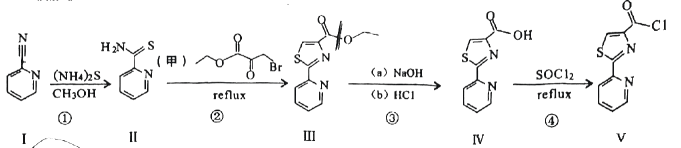
已知:
回答以下问题:
序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
① | 消去反应 | ||
② |
| ||
③ | 氧化反应 |
a.红外光谱显示分子中含一个苯环 b.苯环上仅含两个取代基 c.核磁共振氢谱中峰面积之比为
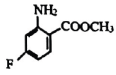 和中间体V为原料,合成
和中间体V为原料,合成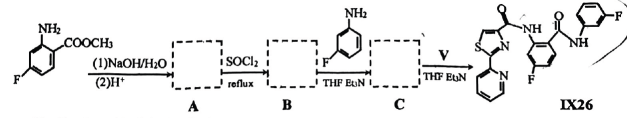
①物质C的结构简式为.
②以物质A为原料合成有机高分子化合物的方程式为.