⑥ , ⑦
, ⑧稀硫酸。按要求回答下列问题:

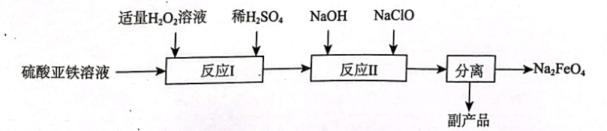
回答下列问题:
+
+
→
+
+
, 该反应中,
被 。(填“氧化”或“还原”)
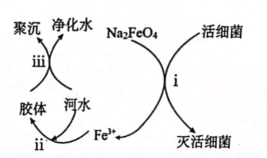
【查阅资料】向胶体中加入电解质后,胶体因失去稳定性而发生离子的聚集以至沉淀,称为电解质对胶体的聚沉作用,简称胶体的聚沉。
①过程i中活细菌表现了。(填“氧化”或“还原”)性,过程ⅲ属于。(填“物理”或“化学”)变化。
②根据上述原理分析,作水处理剂时,的作用有。

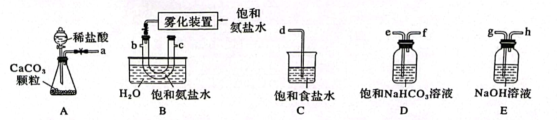
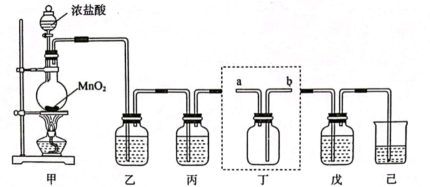
回答下列问题:
已知:溶液呈碱性:
;
①漂白粉中的能与空气中的
和水蒸气反应,从而发生变质,写出该反应的化学方程。
②乙同学认为甲同学的实验无法证明漂白粉是否变质,原因是。
③由乙同学的实验可以证明漂白粉(填“没有变质”、“部分变质”或“完全变质”)