① 取该样品溶于水,得到无色溶液;
② 取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,过滤;
③ 向步骤②所得沉淀中加入过量的HNO3 , 沉淀全部消失并产生气泡。
下列分析中正确的是( )
A | 硫酸亚铁溶液出现棕黄色沉淀 | |
B | 硫化钠溶液出现浑浊颜色变深 | |
C | 溴水颜色逐渐褪去 | |
D | 胆矾表面出现白色粉末 |
实验方案 | 现象 | 结论 | |
A | 往 | 短时间内无明显现象 |
|
B | 往 | 溶液先变成血红色后无明显变化 |
|
C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加 | 溶液呈浅绿色 | 食品脱氧剂样品中没有 |
D | 向沸水中逐滴加5~6滴饱和 | 溶液先变成红褐色再析出沉淀 |
|
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.Na2SO3
Ⅰ.制备氯气和金属氯化物


选项 | Ⅰ | Ⅱ | Ⅲ |
a | 干燥的有色布条 | 生石灰 | 湿润的有色布条 |
b | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |

回答下列问题:
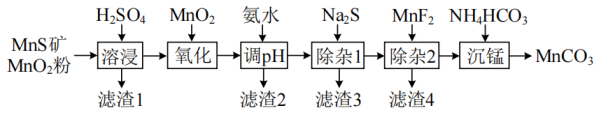
相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | | | | | | | |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |

①写出从开始加热到A点过程中发生反应的化学方程式。
②若D点对应的固体残留率为64.52%,写出D点残留固体的成分及物质的量之比。