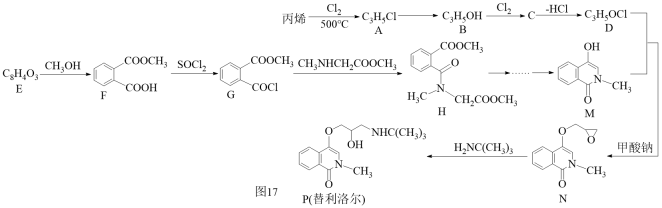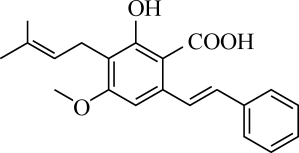
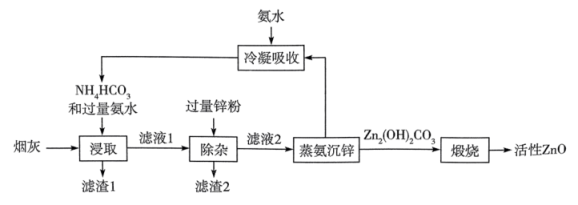
ii.下表是常温下几种离子生成氢氧化物沉淀的pH:
Zn2+ | Fe2+ | Fe3+ | Cu2+ | |
开始沉淀的pH | 5.4 | 7.0 | 2.3 | 4.7 |
完全沉淀的pH | 8.0 | 9.0 | 3.1 | 6.7 |
若以钢铁厂烟灰为原料制备活性ZnO的实验方案设计如下:
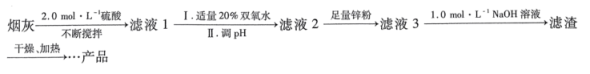
①向滤液1中加入适量双氧水的作用是(用离子方程式表示) ,调pH加入的固体可以是。 (填化学式)。
②向滤液2中加入足量锌粉的目的是;向滤液3中加入1.0mol·L-1NaOH溶液调节的pH范围为。
已知:①青蒿素可溶于乙醇、乙醚,在水中几乎不溶,熔点为156℃~157℃。
②乙醇的沸点为78℃,乙醚的沸点为34.5℃。
③青蒿素受热不稳定。
实验室提取青蒿素流程如图所示。
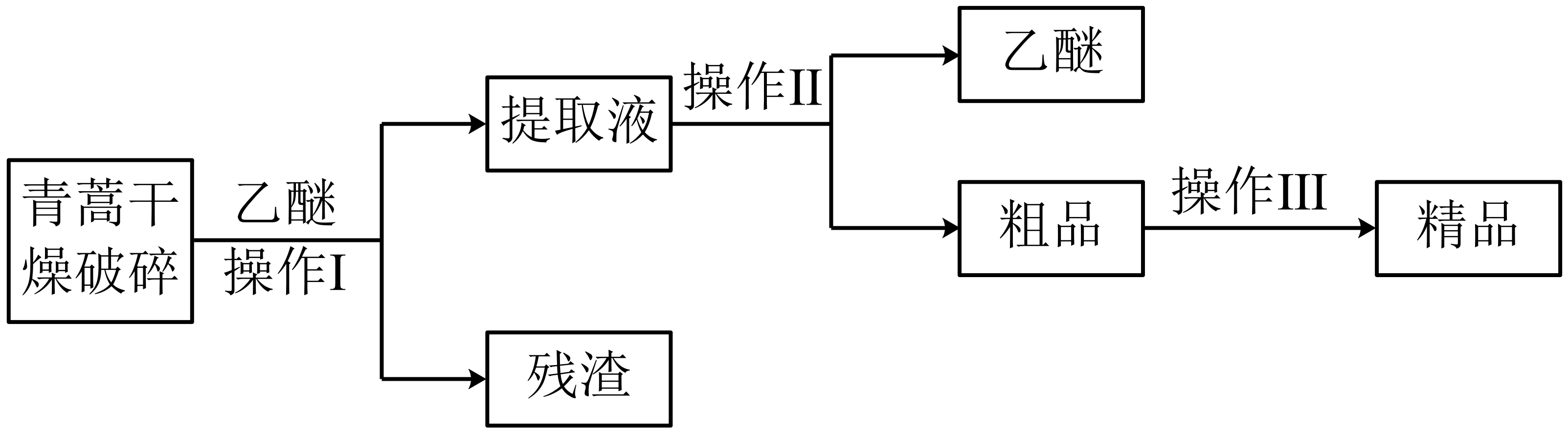
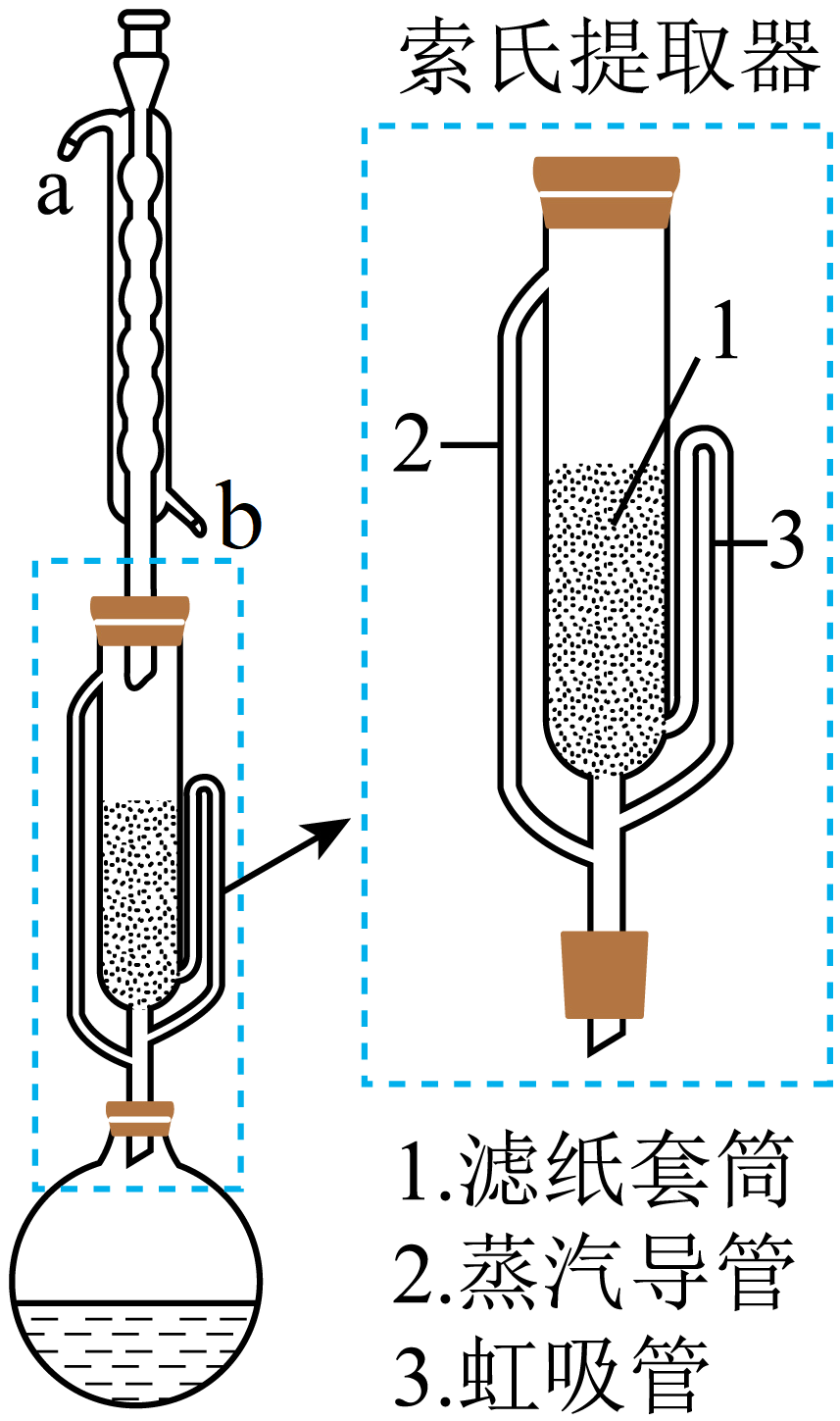
①装置a的名称为。
②索氏提取的青蒿素位于。(填“圆底烧瓶”或“索氏提取器”)中;与常规的萃取相比,索氏提取的优点是。
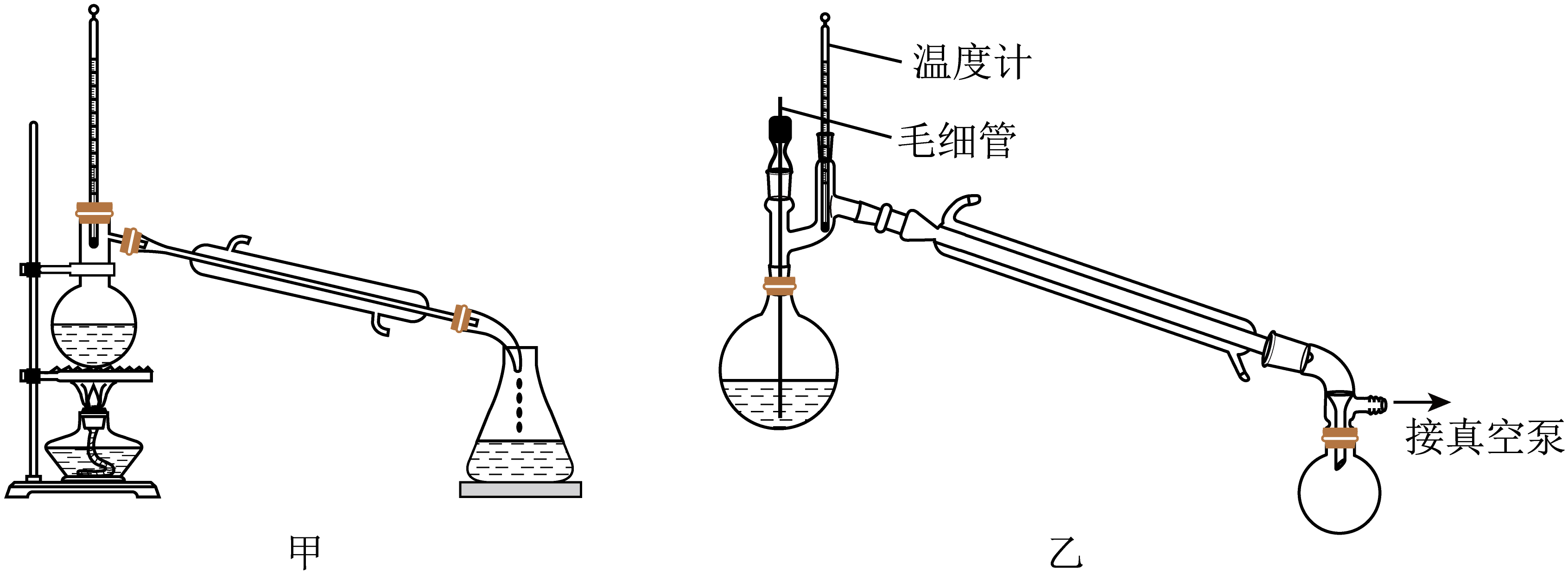
a.加水溶解、蒸发浓缩、冷却结晶
b.加70%的乙醇溶解、水浴加热、冷却结晶、过滤
c.加入乙醚进行萃取分液
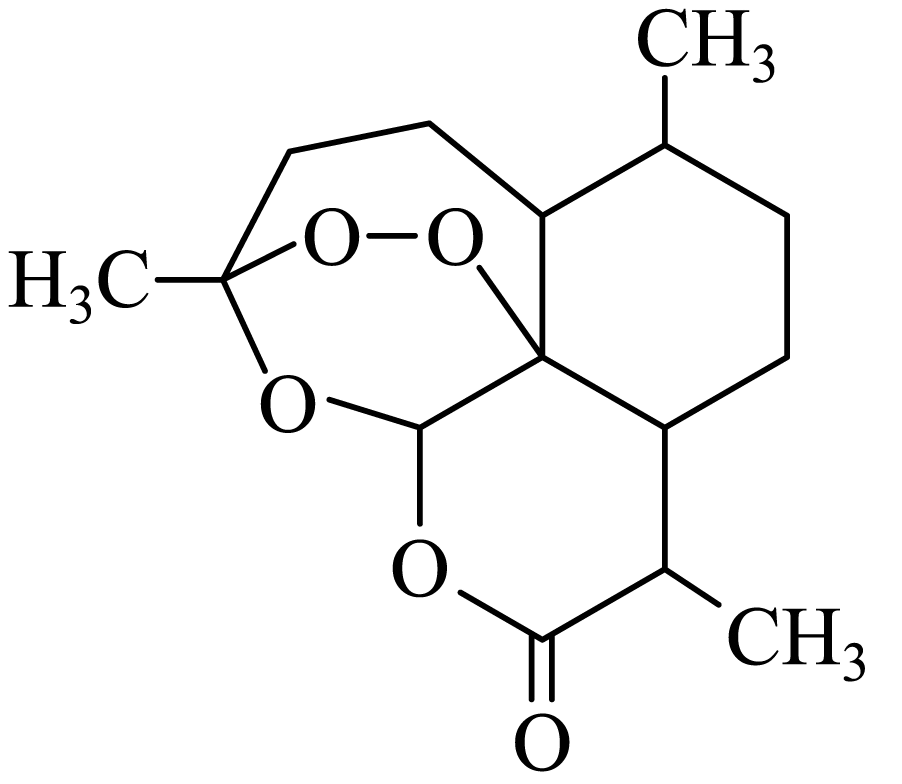 )中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取样品
)中含有过氧键,与碘化钠反应生成碘单质。为测定产品中青蒿素的纯度,取样品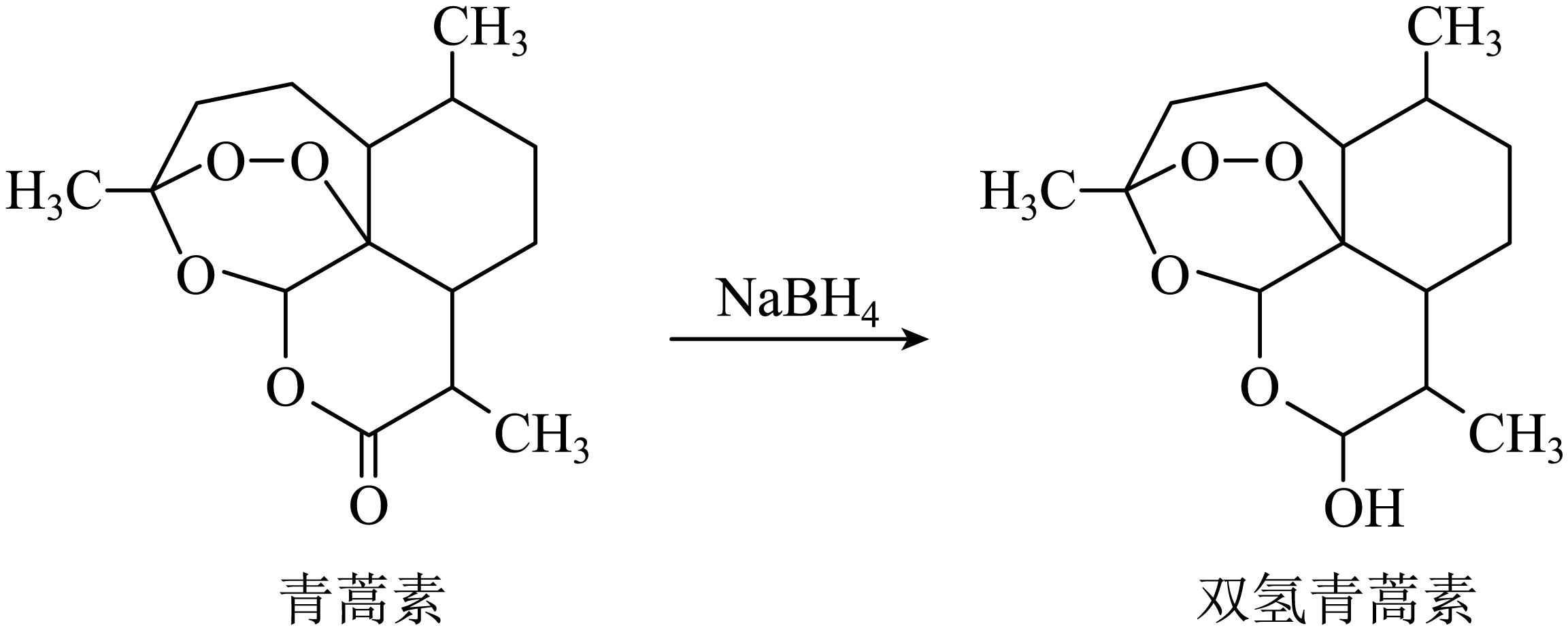
从结构与性质关系的角度推测双氢青蒿素比青蒿素的水溶性、疗效更好的原因:。
H2C2O4 | H2CO3 | HNO2 |
Ka1=5.6×10-2 Ka2=1.5×10-4 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=5.6×10-4 |
回答下列问题:
滴定次数 | 滴定前酸性KMnO4溶液的读数/mL | 滴定后酸性KMnO4溶液的读数/mL |
1 | 0.10 | 20.30 |
2 | 0.50 | 20.80 |
3 | 0.00 | 22.00 |
4 | 1.10 | 21.20 |
①KMnO4溶液应盛装在(填“酸式”或“碱式”)滴定管中,原因为。
②达到滴定终点时的标志为。
③c(H2C2O4)= mol∙L-1。