
①写出与NaOH溶液反应生成两种氮的含氧酸盐的化学方程式:。
②将硝酸尾气中的NO,通入过量的NaOH溶液中充分反应后无气体剩余,则中的x的取值范围是(用含x的式子表示,已知:
)。
实验I:验证乙酸的酸性比碳酸强
某同学设计如下图所示的实验装置,验证乙酸的酸性强于碳酸。

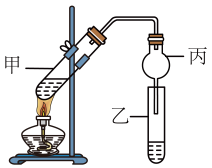
实验Ⅱ:制备乙酸乙酯
该小组同学按图所示装置进行实验,以制取乙酸乙酯。

①A为生物燃料电池的(填“正”或“负”)极。
②正极反应式为。
③放电过程中,H+向极区迁移(填“A”或“B”)。
④在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是,通过外电路的电子是mol。

①工作时,O2-电极移动(填“a”或“b”)。
②电子在外电路中通过传感器的流动方向是(填“由a向b”或“由b向a”)。