
84消毒液 |
(有效成分)NaClO (规格)500mL |
(质量分数)14.9% (密度)1.1g·cm-3 |
①该“84消毒液”有效成分的物质的量浓度为。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因。某消毒小组人员用的浓硫酸配制
的稀硫酸用于增强“84消毒液”的消毒能力,配制该稀硫酸的过程中,除用到量筒、烧杯、玻璃棒及胶体滴管外,还需要的玻璃仪器有。若所配制的稀硫酸浓度偏高,则可能的原因是(填字母)。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.未洗涤烧杯和玻璃棒
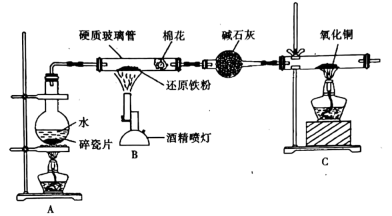
回答下列问题:

①与
分别为(填化学式)。
②加入过量溶液发生反应的离子方程式为。
③写出流程图中溶解的离子方程式。