
①若选择试剂A和D,则甲中发生反应的化学方程式为。
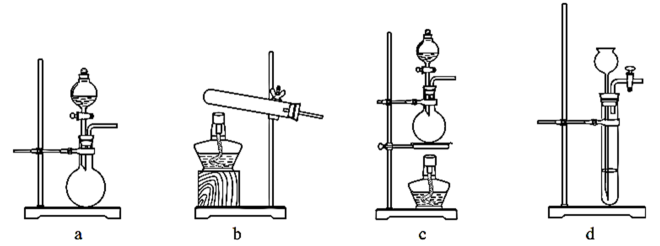
②若只用一种试剂制取氨气,则该试剂的最佳选择为 (选填试剂标号),此时,甲中空白处所需装置应为 (选填下列标号)。
③实验结束后从戊中取出少量液体于试管中,滴入紫色石蕊试液,当观察到现象时,说明已制得硝酸。若没有观察到此现象,可能的原因是。
①实验任务:通过设计实验探究Fe(NO3)3溶液溶解银的原因。
②查阅资料:在不同条件下的还原产物较复杂,有时难以观察到气体产生。
③提出猜想:猜想a:Fe3+具有氧化性,能够氧化Ag;
猜想b:Fe(NO3)3溶液呈酸性,在此酸性条件下能氧化Ag。
④设计实验、验证猜想
Ⅰ. 甲同学从上述实验的生成物中检测出Fe2+ , 验证了猜想a成立。请写出Fe3+氧化Ag的离子方程式。
Ⅱ. 乙同学设计实验验证猜想 , 请帮他完成下表中内容
实验步骤(不要求写具体操作过程) | 预期现象和结论 |
① ② | 若银镜消失,猜想b成立; 若银镜不消失,猜想b不成立。 |

回答下列问题:

已知:①与
同主族,其化学性质相似。
②随着温度升高,在水溶液中的溶解度减小:
温度/ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/ | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
③本工艺流程中,不同金属离子形成氢氧化物沉淀的范围如表格所示:
金属离子 | 形成氢氧化物沉淀的 |
3.3~10.6 | |
2.9~9.4 |
回答下列问题:

回答下列问题:

①图a不是纤锌矿型ZnO的晶胞单元,原因是。
②图b闪锌矿型属于立方晶胞,原子1的坐标为 , 则原子2的坐标为。
③图的闪锌矿型ZnO晶体中离O距离最近的Zn原子数为,其晶胞参数为a nm,阿伏加德罗常数的值为NA , 则晶体密度为g/cm3(列出计算式)。

已知如下信息:
回答下列问题: