|
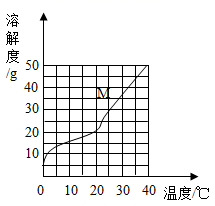
| 0 | 10 | 20 | 30 | 40 |
| 氯化钠 | 35.7 | 35.8 | 36 | 36.5 | 37 |
| 碳酸钠 | 6 | 16 | 18 | 36.5 | 50 |
| 硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
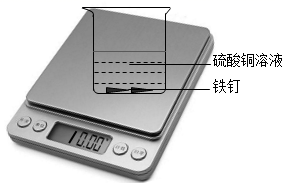
(提出设想)设想一:增大硫酸铜溶液的浓度
设想二:用更活泼的金属锌代替铁钉
(实验验证)小东将以上实验进行了如下改进:
|
实验内容 |
实验现象 |
|
|
实验1 |
烧杯中换成饱和硫酸铜溶液 |
①几小时后溶液颜色几乎不变 ②天平读数不变 ③铁钉表面有变化 |
|
实验2 |
铁钉换成锌粒 |
①溶液颜色明显变浅 ②天平读数减小 ③锌粒表面有变化 |
(实验分析)从以上现象分析,两个设想都不合适,其中按设想(填“一”或“二”)进行的实验能够验证质量守恒定律。
