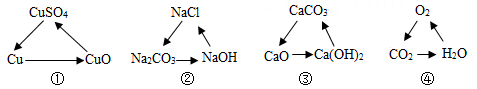
①木炭②白酒③头发④醋酸⑤小苏打⑥蛋清⑦生石灰

|
一些物体的动能 |
|
|
行走的牛 |
约60J |
|
跑百米的运动员 |
约3×102J |
|
飞行的步枪子弹 |
约5×108J |
【实验研究】拉动注射器,让废气依次通过装置。
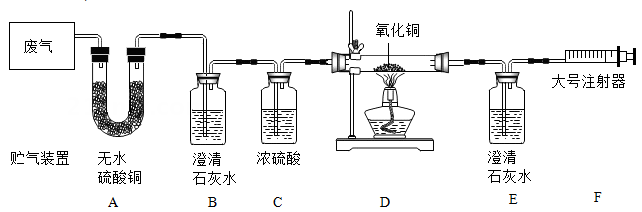
【实验分析】
小金认为,仅根据E中澄清石灰水变浑浊,无法确定一氧化碳的存在,其理由是;
【实验结果】经检验,废气中存在CO2、CO、H2O。
|
实验次数 |
1 |
2 |
3 |
4 |
|
稀硫酸的用量/克 |
20 |
20 |
20 |
20 |
|
剩余固体的质量/克 |
20.0 |
17.4 |
14.8 |
13.5 |
分析上述数据,请回答下列问题: